
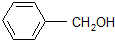 ③
③ ④
④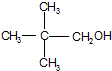
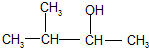 ⑥
⑥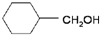 ⑦CH3-CH2-O-CH2-CH3
⑦CH3-CH2-O-CH2-CH3

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、S2-、Al3+、ClO-、Cl- |
| B、K+、Mg2+、OH-、NO3- |
| C、H+、Mg2+、SiO32-、SO42- |
| D、NH4+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c2(H2)?c(CO2) |
| c2(H2O) |
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
| 催化剂 |
投料比[
|
500K | 600K | 700K | 800K | ||
| 1.5 | 45% | 33% | 20% | 12% | ||
| 2.0 | 60% | 43% | 28% | 15% | ||
| 3.0 | 83% | 62% | 37% | 22% |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、该原电池中,铜为正极 |
| B、该原电池中,电子由铜片经过导线流入锌片 |
| C、该原电池工作一段时间后,溶液的酸性减弱 |
| D、该原电池工作一段时间后,锌片质量减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 |
 |
 |
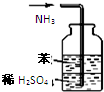 |
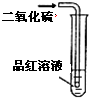
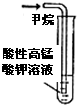
| ① | ② | ③ | ④ |
| A、实验①溶液褪色 |
| B、实验②溶液褪色 |
| C、实验③电流计发生偏转 |
| D、实验④氨气能被安全吸收 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com