
| A. | 容量瓶使用前用1.0mol•L-1的Na2CO3溶液润洗 | |
| B. | 配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 | |
| C. | 仰视确定凹液面与刻度线相切 | |
| D. | 定容摇匀后,发现液面低于刻度线,又补加蒸馏水至刻度线 |
分析 结合c=$\frac{n}{V}$及不当操作对n、V的影响判断浓度变化,n偏大或V偏小则导致溶液浓度偏高,以此来解答.
解答 解:A.容量瓶使用前用1.0mol•L-1的Na2CO3溶液润洗,n偏大,则浓度偏高,故A正确;
B.未用蒸馏水洗涤烧杯和玻璃棒,n偏小,浓度偏低,故B错误;
C.仰视确定凹液面与刻度线相切,V偏大,浓度偏低,故C错误;
D.定容摇匀后,发现液面低于刻度线,又补加蒸馏水至刻度线,V偏大,浓度偏低,故D错误;
故选A.
点评 本题考查配制一定浓度的溶液,为高频考点,把握浓度公式及不当操作为解答的关键,侧重分析与实验能力的考查,注意结合公式分析误差,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 过滤时,玻璃棒靠在三层滤纸边沿稍下方 | |
| B. | 配制一定物质的量浓度的溶液,在移液时玻璃棒轻靠在容量瓶瓶口 | |
| C. | 测定烧杯中溶液的pH时,用pH试纸直接在烧杯中蘸取溶液 | |
| D. | 做酸碱中和滴定实验时,眼睛一直紧盯装有标准液的滴定管,防止液面低于刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL 2mol/L MgCl2溶液 | B. | 1000mL 2.5mol/L NaCl溶液 | ||
| C. | 300mL 5mol/L NaClO溶液 | D. | 250mL 1mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑦ | B. | ①②⑥⑧ | C. | ①③④⑧ | D. | ①③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
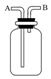
| A. | 瓶中盛满水,从B口进气,用排水法收集NO2 | |
| B. | 瓶中盛适量浓硫酸,从A口进气来干燥NH3 | |
| C. | 从A口进气,用排空气法收集CO2 | |
| D. | 瓶中装满水,B口连导管并伸入量筒中,从A口进气,用排水法测量生成H2的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu丝--电解质;KOH--电解质 | |
| B. | NaCl--电解质;葡萄糖(C6H12O6)--非电解质 | |
| C. | NaCl溶液--非电解质;酒精--非电解质 | |
| D. | O2--不属于电解质或非电解质;MgCl2--非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(D)=6 mol•(L•min)-1 | B. | v(C)=0.5 mol•(L•s)-1 | ||
| C. | v(B)=0.6 mol•(L•s)-1 | D. | v(A)=0.15 mol•(L•s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| -c(NO)/mol•L -1 | 1.00×10 -3 | 4.50×10-4 | 2.50×10 -4 | 1.50×10 -4 | 1.00×10 -4 | 1.00×10 -4 |
| -c(CO)/mol•L-1 | 3.60×10 -3 | 3.05×10 -3 | 2.85×10 -3 | 2.75×10 -3 | 2.70×10 -3 | 2.70×10-3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com