
ѡ���Դ���ԭ(SCR)�����д����������½�NOx ת��ΪN2��H2O������Ŀǰ�������᳧����β���������ձ���õ�һ�ַ�����
ijУ�ס���������ѧ��ȤС������֤NO�ܱ�������ԭ��������ת���ʡ�
��һ����������ȡ�����Ǹ���ͭ����
�Ǹ���ͭ��Adkin�������Ǽ��õ�NO����ԭ�Ĵ�������ͭ���ĸ���������ɷֲ��̶����磺CuO��Cr2O3�ȣ�ͳ��Ϊ�Ǹ���ͭ������ͬѧȡһ��������ͭ��Һ�������������ᱵ���ȶ������� �ظ������Һ�백ˮ���õ�����ɫ������ ��������[���ⶨΪ����ʽ����ͭ泥�CuNH4(OH)CrO4 )]���ˡ�ϴ�ӣ�80����12h�� ����ա�
��1�������õ��IJ��������У� �� ��ѡ����ţ���ͬ���������õ��������У� �� ��
A�������� B��ʯ���� C�������� D���ձ� E������ǯ F���ƾ���
G�������� H��©�� I��������������������ȥ��
��2��CuNH4(OH)CrO4��295��ֽ����ɸ��ϵ��������������������ˮ���÷�Ӧ�Ļ�ѧ����ʽ: �� ��
�������������ü����Ƶô������������̽���ʵ�顣
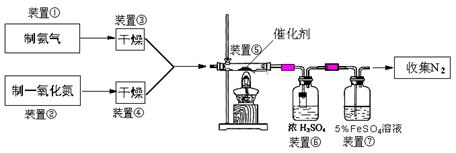
�Իش��������⣺
��3������ȡ������Aװ�ã�������Ӧ�Ļ�ѧ����ʽΪ�� �� ��
����Bװ����ȡ���������Һ©������ƿ��ʢ�ŵ�ҩƷ�ֱ��ǣ� �� ��
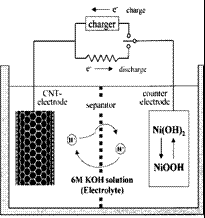
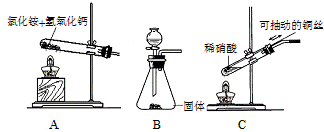
��4����ͼCװ����ȡNOʱ���ÿɳ鶯��ͭ˿���ŵ��ǣ� �� ��
��5��װ�âߵ����ÿ������� �� ��
��6��������װ�âݵ�NO��2688mL��������Ϊ��״������ͬ������������������ռ�����״����2016mLN2����NO��ת����Ϊ�� �� ��
��1��D��G��H �� C��E��F��G��I����ѡ��ѡ�������֣���
��2��2Cu(OH)NH4CrO4![]() Cr2O3��2CuO+N2��+5H2O������д��������ƽ�����֣���
Cr2O3��2CuO+N2��+5H2O������д��������ƽ�����֣���
��3��2NH4Cl+Ca(OH)2![]() CaCl2+2NH3�� +2H2O��Ũ��ˮ����ʯ��(��ʯ�һ��������ƹ���)
CaCl2+2NH3�� +2H2O��Ũ��ˮ����ʯ��(��ʯ�һ��������ƹ���)
��4����Ӧ������ʱ��ͣ���������㡢����ʹ�á���ԼҩƷ��
��5������δ��Ӧ��NO
��6��90%
���ڰѻ���ʵ��֪ʶ�������龰�dz������ⷽʽ���������ڼ��⣬��1����3�����ʿ�ֱ�ӻش𣻣�2������Ҫ�õ��龰��CuO��Cr2O3��Ϊ��Ӧ�IJ�����������ֿ�����������ԭ��Ӧ�����һ�ʽⷨ�����õ�Ԫ���غ㣺�ɷ�Ӧ����ʽ4NH3+6NO=5N2+6H2O��֪��������2016mL��0.09mol N2ʱ����ҪNO 0.108mol
��NOΪ0.12 mol������ת����Ϊ90%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
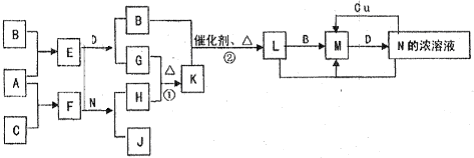


| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NOX��Ҫ����������β�����ŷţ�����������ЧӦ����Ҫ����֮һ | B��N2�Ц�����O��֮��Ϊ1��2 | C����Ӧ����ÿ����22.4LN2��ת�Ƶ�����1.5NA | D��NH3�ķе��PH3�ķе�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
(12��)ѡ���Դ���ԭ(SCR)�����д����������½�NOx ת��ΪN2��H2O������Ŀǰ�������᳧����β���������ձ���õ�һ�ַ�����
.ijУ�ס���������ѧ��ȤС������֤NO�ܱ�������ԭ��������ת���ʡ�
��һ����������ȡ�����Ǹ���ͭ����
�Ǹ���ͭ��Adkin�������Ǽ��õ�NO����ԭ�Ĵ�������ͭ���ĸ���������ɷֲ��̶����磺CuO?Cr2O3�ȣ�ͳ��Ϊ�Ǹ���ͭ������ͬѧȡһ��������ͭ��Һ�������������ᱵ���ȶ��������ظ������Һ�백ˮ���õ�����ɫ������ ��������[���ⶨΪ����ʽ����ͭ泥�CuNH4(OH)CrO4 )]���ˡ�ϴ�ӣ�80����12h�� ����ա�
��1�������õ��IJ��������У� ��ѡ����ţ���ͬ���������õ��������У� ��
A�������� B��ʯ���� C�������� D���ձ� E������ǯ F���ƾ���
G�������� H��©�� I��������������������ȥ��
��2��CuNH4(OH)CrO4��295��ֽ����ɸ��ϵ��������������������ˮ���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�������������ü����Ƶô������������̽���ʵ�顣
![]()

�Իش��������⣺
��3������ȡ������Aװ�ã�������Ӧ�Ļ�ѧ����ʽΪ�� ������Bװ����ȡ���������Һ©������ƿ��ʢ�ŵ�ҩƷ�ֱ��ǣ� ��
![]()

��4����ͼCװ����ȡNOʱ���ÿɳ鶯��ͭ˿���ŵ��ǣ� ��
��5��װ�âߵ����ÿ������� ��
��6��������װ�âݵ�NO��2688 mL��������Ϊ��״������ͬ������������������ռ�����״����2016 mL N2����NO��ת����Ϊ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com