
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为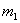 g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:镁铝合金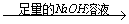 充分反应后测定剩余固体质量
充分反应后测定剩余固体质量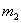 g
g
实验设计2:镁铝合金 生成的气体在标准状况下的体积为VL。
生成的气体在标准状况下的体积为VL。
请回答以下问题:
实验设计1:
(1)镁的质量分数: 。
(2)在溶解、过滤中使用的玻璃仪器有 __________ 。
(3)过滤后洗涤沉淀的操作方法是________________________________________
____________________________________________________。
(4)如果过滤得到沉淀没有用蒸馏水洗涤数次后,烘干,再测定剩余固体质量。测得镁的质量分数量会 (填“偏大”、“偏小”或“无影响”)。
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源:志鸿系列全优设计必修一化学鲁科版 鲁科版 题型:058
含镁3%~5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:
镁铝合金![]() 溶液
溶液![]() 得到沉淀的质量为m2g;
得到沉淀的质量为m2g;
实验设计2:
镁铝合金![]() 生成的气体在标准状况下的体积为V1L.
生成的气体在标准状况下的体积为V1L.
实验设计3:
镁铝合金![]() 生成的气体在标准状况下的体积为V2L.
生成的气体在标准状况下的体积为V2L.
请完成以下问题:
(1)写出实验设计1中单质铝发生反应的离子方程式:________.
(2)写出实验设计2中反应的离子方程式:________.
(3)判断这几种实验设计能否求出镁的质量分数,能求出的用题目提供的数据将镁的质量分数表示出来,不能求出的就空着不填.
①实验设计1________.
②实验设计2________.
③实验设计3________.
查看答案和解析>>
科目:高中化学 来源:新人教版2012届高三上学期单元测试(5)化学试题 人教版 题型:058
铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
[方案一]
[实验方案]将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.
实验中发生反应的化学方程式是________.
[实验步骤]
(1)称取5
.4 g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中.为使其反应完全,则NaOH溶液的体积V≥________.(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将________(填“偏高”、“偏低”或“无影响”).
[方案二]
[实验方案]将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1
.01×105 Pa)的体积.[问题讨论]
(1)同学们拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因________.
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是________.
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了下图所示的实验装置.

①装置中导管a的作用是________.
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL.则产生氢气的体积为________mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计以下实验方案进行探究。填写下列空白。
[实验方案] 铝镁合金粉末![]() 测定剩余固体质量
测定剩余固体质量
[实验步骤]
步骤1:称取5.4g铝镁合金粉末样品,投入VmL 2.0mol·L—1NaOH溶液中,充分反应。
步骤2:过滤、洗涤、干燥、称量固体。
[交流与讨论]
(1) 实验中发生反应的化学方程式是 ;
(2)参与反应的NaOH溶液的体积V≥ ;
(3)步骤2中,如果经两次过滤滤液仍浑浊,则原因可能是_________(只填一点);
(4)步骤2中,若未洗涤固体,测得镁的质量分数将 (填“偏高”或“偏低”)。
[实验拓展] 请你另设计一个实验方案(用上述方案的试剂),测定该铝镁合金中镁的质量分数。
要求:从下图中挑选所需的仪器,画出该方案的实验装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明所用试剂.


查看答案和解析>>
科目:高中化学 来源: 题型:
铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
【探究一】实验方案:铝镁合金![]() 测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是
实验步骤:
(1)称取5.4g 铝镁合金粉末样品,投入VmL 2.0 mol?L-1 NaOH溶液中,充分反应。NaOH溶液的体积V≥
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
(填“偏高”或“偏低”)。
[探究二]
实验方案:铝镁合金![]() 测定生成气体的体积实验装置:
测定生成气体的体积实验装置:

问题讨论:
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置。你的意见是: (填“需要”或“不需要”)。
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
① ②
[探究三]
实验方案:称量x g铝镁合金粉末.放在如下图所示装置的惰性电热板上,通电使其充分灼烧。

问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是
(2)若用空气代替O2进行实验,对测定结果是否有影响? (填“是”或“否”)。
[实验拓展]
参照探究一、探究二实验方案,请你另设计一个实验方案,测定该铝镁合金中镁的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为![]() g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:镁铝合金![]() 充分反应后测定剩余固体质量
充分反应后测定剩余固体质量![]() g
g
实验设计2:镁铝合金![]() 生成的气体在标准状况下的体积为VL。
生成的气体在标准状况下的体积为VL。
请回答以下问题:
(1) 实验设计1:
①镁的质量分数: 。
②在溶解、过滤中使用的玻璃仪器有 __________ 。
③过滤后洗涤沉淀的操作方法是________________________________________
____________________________________________________。
④如果过滤得到沉淀没有用蒸馏水洗涤数次后,烘干,再测定剩余固体质量。测得镁的质量分数量会 (填“偏大”、“偏小”或“无影响”)。
(2)  实验设计2:测定生成的气体装置如右图,
实验设计2:测定生成的气体装置如右图,
进行的操作有:
a.记录C的液面位置;
b.待B中不再有气体产生并恢复至室温后,记录C的液面位置;
c.检查气密性;
d.将药品和水装入各仪器中,连接好;
e.由A向B中滴加足量试剂。
①上述操作的顺序是:_______________________________(填序号)。
②记录C的液面位置时,除视线平视外,还应注意:
___________________________________________________________。
![]()
![]() (3)请你利用实验设计1和实验设计2的模式再设计一个实验方案:
(3)请你利用实验设计1和实验设计2的模式再设计一个实验方案:
铝镁合金 ![]() 溶液
溶液 ![]() 过滤,测定质量。
过滤,测定质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com