
һ�������£������Ϊ10L���ܱ������У�1 molX��1 molY������Ӧ��2x��g��+Y��g�� Z��g������60s�ﵽƽ�⣬����0��3mol Z������˵����ȷ����
Z��g������60s�ﵽƽ�⣬����0��3mol Z������˵����ȷ����
| A����Ӧ����30 sʱ������Ӧ���ʵ����淴Ӧ���� |
| B����Ӧ����80 sʱ���淴Ӧ���ʴ�������Ӧ���� |
| C����Ӧ����60 sʱ��X�����ʵ���Ũ��Ϊ0��04 mol/L |
| D����Ӧ����60 sʱ��Y��ת����Ϊ70�� |
C
�������������A�����ڷ�Ӧ��60s�ﵽƽ�⣬�����ڷ�Ӧ����30 sʱ������Ӧ���ʴ����淴Ӧ���ʣ�����B�����ڷ�Ӧ��60s�ﵽƽ�⣬��Ӧ����80 sʱ�������������ȱ仯����ƽ�Ᵽ�֣��淴Ӧ���ʵ�������Ӧ���ʣ�����C����Ӧ����60 sʱ������0��3mol Z �����ݷ�Ӧ����ʽ�и�������֮��Ĺ�ϵ����֪��X����0��6mol������0��4mol��X����X�����ʵ���Ũ��Ϊ0��4mol ��10L=0��04 mol/L����ȷ��D����Ӧ����60 sʱ���ﵽƽ�⣬���ݷ���ʽ��Y��Z�Ĺ�ϵ��֪��Ӧ����Z�����ʵ�����0��3mol����Y��ת����Ϊ(0��3mol ��1mol)��100%=30����
���㣺������淴Ӧ�еĻ�ѧ��Ӧ���ʺͻ�ѧƽ�⡢���ʵ�ת���ʵ�֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ijʵ��С�������50 mL 1.0 mol/L�����50 mL 1.1 mol/L ����������Һ����ͼװ���н����кͷ�Ӧ���ڴ��ձ��ײ�������ĭ����(��ֽ��)��ʹ�����С�ձ���������ձ�������ƽ��Ȼ�����ڴ�С�ձ�֮����������ĭ����(��ֽ��)�����ձ�������ĭ���ϰ�(��Ӳֽ��)���ǰ壬�ڰ��м俪����С�ף�����ʹ�¶ȼƺͻ��β��������ͨ����ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��Իش��������⣺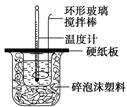
��1����ʵ�������Թ�����NaOH��ԭ��̲���˵��Ϊ��֤������ȫ���к͡����ʣ������ڷ�Ӧ������Ϊ�з�������������������ڷ�Ӧ�лӷ������õ��к��� (�ƫ����ƫС�����䡱)��
��2�����к��Ȳⶨʵ���д�����ˮϴ���¶ȼ��ϵ�����IJ��裬���˲������裬���õ��к��Ȼ� (�ƫ����ƫС�����䡱)��
��3�����õ�Ũ�ȵĴ�����NaOH��Һ��Ӧ�����õ��к��Ȼ� (�ƫ����ƫС�����䡱)����ԭ���� ��
��4����ʵ��С����������ʵ�飬ÿ��ȡ��Һ��50 mL������¼��ԭʼ����(���±�)��
| ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�(t2)/�� | �²�(t2��t1)/�� | ||
| ���� | NaOH��Һ | ƽ��ֵ | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���¶Ȳ���������£��ں��ݵ������н������з�Ӧ��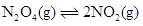 ����
����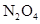 ��Ũ����
��Ũ����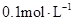 ����
����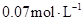 ��Ҫ15s����ô
��Ҫ15s����ô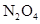 ��Ũ����
��Ũ����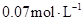 ����
����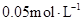 ����ķ�Ӧʱ�䣨 ��
����ķ�Ӧʱ�䣨 ��
| A������5s | B������10s | C������10s | D����10s |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��10L�ܱ������У�A��B��C������̬���ʹ��ɿ��淴Ӧ��ϵ�����ϵ��ͼ��ʾ������˵��������ǣ� ��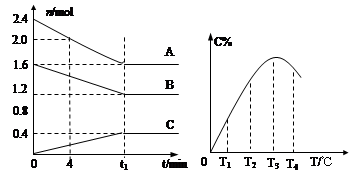
A��0��4����ʱ��A��ƽ����Ӧ����Ϊ 0.01mol��L-1��min-1
B����T1��T2�仯ʱ��V����V��
C���˷�Ӧ������ӦΪ���ȷ�Ӧ
D�������������䣬��ѹ������ƽ��ʱ��C�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���¶��£�10 mL 0.40mol/LH2O2��Һ�������ֽ⡣��ͬʱ�̲������O2�������������Ϊ��״�������±���������������ȷ���ǣ���Һ����仯���Բ��ƣ�
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V��O2��/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪X��g��+3Y��g���T 2Z��g����H��0�����жԸ÷�Ӧ��˵������ȷ����
| A����S��0 |
| B���������Է����У��ҷ�Ӧ���ʺ�ƽ�ⳣ�����ϴ� |
| C����Ӧ������������������������ |
| D�����κ��¶��¶������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��þ��Ͷ��ʢ������ij���������������ضԷ�Ӧ������Ӱ�����
�������Ũ�� ��þ���ı���� ����Һ���¶� �������ӵ�Ũ��
| A���٢� | B���ۢ� | C���٢ڢۢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ͼΪװ�л������������Բ��ƣ����ܱ���������ʢ22��4mLһ����������ͨ��11��2mL����(����������ڱ�״���²ⶨ)�������¶�ѹǿ���䣬�������ڵ��ܶ�Ϊ����ʾ��������NOת��ΪNO2�Ŀ����ԣ�
| A������1��369 g��L-1 |
| B������2��054 g��L-1 |
| C����1��369g��L-1��2��054g��L-1֮�� |
| D����2��054g��L-1��4��108g��L-1֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�����º��ݵ��ܱ������з������·�Ӧ��2A(g)+ B(s)  C(g)+3D(g)������˵���÷�Ӧ�ﵽƽ�����( )
C(g)+3D(g)������˵���÷�Ӧ�ﵽƽ�����( )
| A���������������� | B����������ܶȲ��� |
| C����Ӧ��B��Ũ�Ȳ��� | D���������ƽ����Է����������ٸı� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com