
有人设计以Pt和Zn为电极材料,埋入人体内作为某种心脏病人的心脏起搏的能源。它依靠人体内含有一定浓度的溶解氧进行工作,下列叙述中错误的是( )
A.Pt是正极
B.负极反应:Zn-2e-===Zn2+
C.正极反应:2H++2e-===H2↑
D.正极反应:2H2O+O2+4e-===4OH-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某化学兴趣小组使用右图所示装置,对某种铁铜合金的成分
 进行测量。先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品
进行测量。先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品
开始计时,并将电子天平的读数记录在下表中,请回答下列问题:
⑴ 根据电子天平读数和时间的关系分析,该反应进行过程中,
氢气的产生速度有什么特点?
⑵ 完全反应后,烧杯中盐的质量分数为多少?(用百分数表示)
⑶ 合金中铁元素的质量百分含量为多少?
| 空烧杯 | 加入 硫酸后 | 加入铁粉后5分钟 | 加入铁粉 | 加入铁粉后21分钟 | 加入铁粉后40分钟 | 加入铁粉后3小时 | |
| 读数(g) | 28.5 | 169.7 | 183.6 | 183.5 | 183.4 | 183.3 | 183.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在烧杯中的盛有10g H Cl和BaCl2溶液,向其中逐滴滴入溶质质量分数为13.25%
Cl和BaCl2溶液,向其中逐滴滴入溶质质量分数为13.25%
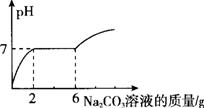
的碳酸钠溶液。测得溶液pH与加入的碳酸钠溶液的质量关系如图所示。
(1)通过图中可知,当碳酸钠溶液质量加到 g时,溶液中盐酸恰好完全反应。
 (2)请计算原烧杯溶液中氯化钡的质量分数。
(2)请计算原烧杯溶液中氯化钡的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阳离子的说法中错误的是( )
①阳离子都是由一个金属原子失去电子而形成的 ②非金属原子不能形成阳离子 ③阳离子的电子排布一定与稀有气体元素原子相同 ④阳离子的价态不会大于其原子的最外层电子数 ⑤阳离子都是稳定结构,不会再失去电子
A.①④ B.②④
C.①②③ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.电解饱和食盐水,阳极的电极反应式为:2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电池正极相连的是纯铜,电极反应式为:Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
可再生能源是我国重要的能源资源,在满足能源需求、改变能源结构,减少环境污染、促进经济发展等方面具有重要作用。应用太阳能光伏发电技术,是实现节能减排的一项重要措施。
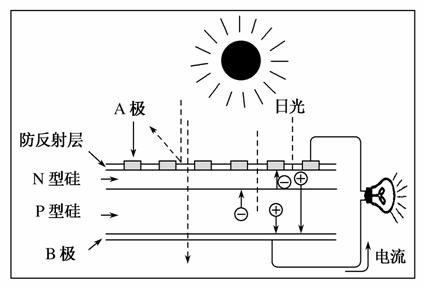
下列分析不正确的是( )
A.风能、太阳能、生物质能等属于可再生能源
B.推广可再生能源有利于经济可持续发展
C.上图是太阳能光伏电池原理图,图中A极为正极
D.光伏发电池能量转化方式是太阳能直接转变为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
酸、碱、盐溶液能够导电,是因为物质溶于水时,离解成为自由移动的阴、阳离子。
(1)在酸的溶液里,酸根离子所带________的总数等于酸电离时生成的________的总数;在碱的溶液里,跟金属离子结合的________的总数等于这种金属离子所带的________的总数;在盐的溶液中,金属离子所带的________的总数等于酸根离子所带的________的总数。
(2)下列物质的电离方程式如下:
HClO4===H++ClO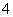 ;
;
Ba(OH)2===Ba2++2OH-;
Fe2(SO4)3===2Fe3++3SO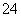 ;
;
KHSO4===K++H++SO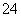 。
。
属于酸的物质________(写化学式);属于碱的物质为________;属于盐的物质________。
(3)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是________。
②上述物质中既不是电解质也不是非电解质的是________。依据是________________________。
③写出纯碱的电离方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是( )
A. X、Y元素的金属性X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C. Y的最高价氧化物的水化物能溶于稀氨水
D.X的最高价氧化物的水化物能与Z的最高价氧化物的水化物发生中和反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com