
【题目】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义。
(1)用CO可以合成甲醇。已知:
CH3OH(g)+3/2O2(g)===CO2(g)+2H2O(l) ΔH=-764.5 kJ·mol-1
CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
则CO(g)+2H2(g) ![]() CH3OH(g) ΔH=______kJ·mol-1。
CH3OH(g) ΔH=______kJ·mol-1。
(2)下列措施中能够增大上述合成甲醇反应速率的是________(填写序号)。
a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将CH3OH从反应混合物中分离出来
(3)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系
如右图所示。
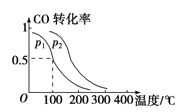
①p1________p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=________;
③在其他条件不变的情况下,再增加a mol CO和2a mol H2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”)。
(4)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:_____________________。
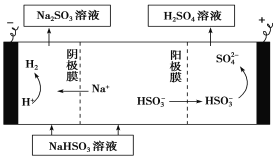
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下。请写出开始时阳极反应的电极反应式:_________________。
【答案】(1)-90.1
(2)ac
(3)①小于 ②(V/a)2(2分) ③增大
(4)①SO2+2H2O-2e-===SO42-+4H+
②HSO3-+H2O-2e-===SO42-+3H+
【解析】
试题分析:(1)
①CH3OH(g)+3/2O2(g)===CO2(g)+2H2O(l) ΔH=-764.5 kJ·mol-1
② CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
③H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
根据盖斯定律,②+2×③-①得CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
ΔH=-283.0-285.8×2+764.5 =-90.1kJ·mol-1;
(2)下列措施中能够增大上述合成甲醇反应速率的是ac。
a.使用高效催化剂能加快反应速率
b.降低反应温度,使反应速率减慢
c.增大体系压强,能加快反应速率
d.不断将CH3OH从反应混合物中分离出来,浓度减小,速率减慢;
(3)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如右图所示。①增大压强,平衡向气体系数和减小的方向移动,CO的转化率增大,所以p1小于p2;
②
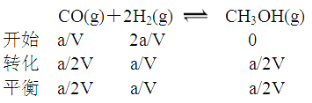
100 ℃时,该反应的化学平衡常数K=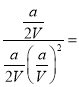 (V/a)2;
(V/a)2;
③在其他条件不变的情况下,再增加a mol CO和2a mol H2,相当于加压,平衡正向移动,达到新平衡时,CO的转化率增大。
(4)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。电池负极发生氧化反应,电池负极的电极反应式:SO2+2H2O-2e-===SO42-+4H+。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解池阳极发生氧化反应,阳极反应的电极反应式:HSO3-+H2O-2e-===SO42-+3H+。


科目:高中化学 来源: 题型:
【题目】有机物中,有一些分子式符合通式CnHn,如C2H2、C6H6等。
(1)关于这些有机物的说法中正确的是______(填编号)。
A.可能互为同系物 |
B.在空气中燃烧时火焰明亮且产生黑烟 |
C.一定能使高锰酸钾酸性溶液褪色 |
D.等质量的这些有机物完全燃烧时耗氧量相同 |
(2)写出分子式为C4H4且为链烃的有机物的结构简式__________,它的一氯代物的同分异构体有________种。
(3)写出除苯外分子式为C6H6且结构中只有C—C键和C—H键的有机物的结构简式:____________________________________________________________。
(4)某有机物分子式为C8H8,且属于芳香烃,已知它可使高锰酸钾酸性溶液和溴水褪色,则该有机物的结构简式为________,写出其发生加聚反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为治理环境,减少雾霾,应采取措施减少二氧化硫、氮氧化物(NOx)和CO2的排放量。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ· mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ· mol-1
②CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH2=-586.7 kJ· mol-1
N2(g)+CO2(g)+2H2O(g) ΔH2=-586.7 kJ· mol-1
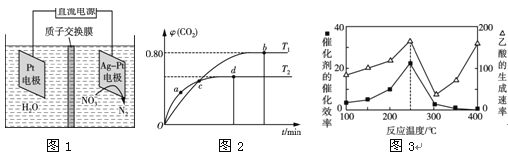
(1)若用4.48 L CH4还原NO生成N2,则放出的热量为 kJ(保留两位小数)。(气体体积已折算为标准状况下)
(2)用电化学处理含NO3—的废水,电解的原理如图1所示,则电解时阴极的电极反应式为 ;
Ⅱ.利用I2O5消除CO污染的反应为5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入4 mol CO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入4 mol CO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
(3)T1时,该反应的化学平衡常数的数值为 。
(4)下列说法不正确的是 (填字母)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,在原容器中充入一定量氦气,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
Ⅲ.以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g)![]() CH3COOH(g) ΔH<0直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图3所示。
CH3COOH(g) ΔH<0直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图3所示。
(5)250~300 ℃时,乙酸的生成速率减小的主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列说法中错误的是( )
A.32 g O2所含的分子数目为NA
B.1 mol H2O含有的H2O分子数目为NA
C.1 mol H2O含有的氢原子数目为NA
D.0.5NA个O2分子的物质的量是0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ下列单元操作中采用了热交换设计的有
A.电解食盐水制烧碱 |
B.合成氨中的催化合成 |
C.硫酸生产中的催化氧化 |
D.氨碱法中的氨盐水碳酸化 |
Ⅱ海水晒盐的卤水中还有氯化镁,以卤水为原料生产镁的一中工艺流程如下图所示。
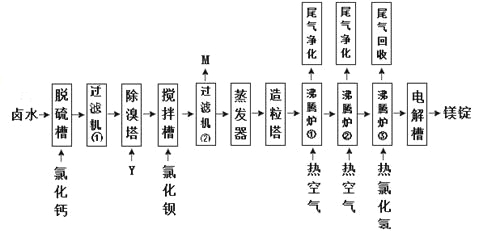
回答下列问题:
(1)脱硫槽、搅拌槽均用于脱除卤水中的(填离子符号),M的主要成分是(填化学式)。
(2)除溴塔中主要的离子方程式为。
(3)沸腾炉①和②的主要作用是。沸腾炉③通入热氯化氢的主要目的是。
(4)电解槽中阴极的电极反应方程式为。
(5)电解槽中阳极产物为,该产物可直接用于本工艺流程中的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有通式均为(CH2O)n的六种有机物,性质如下:
①A是无色有刺激性的气体,可发生银镜反应
②B、C、D的式量均为A的2倍,E的式量的是A的3倍,F的式量是A的6倍
③B、E的水溶液可使紫色石蕊试液变红,还可与乙醇在一定条件下酯化
④E结构中含有—CH3,两分子E 可形成环状酯
⑤C不溶于水,D、F二种物质的水溶液均呈中性,C既能水解,又能发生银镜反应,D不能发生水解反应,却能发生银镜反应,还能与钠反应放出H2,F能发生银镜反应,淀粉水解可得F。
(1)请推断各物质的结构简式:
A ______________、 B__________________、 C ______________、D_______________、 E__________________、 F________________。
(2)请分别写出符合下列要求的E的同分异构体的结构简式:
①能发生银镜反应和酯化反应,又能发生水解反应 ;
②能发生银镜反应和酯化反应,不能发生水解反应 ;
(3)写出A发生银镜反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 NA为阿伏加德罗常数的值。有关草酸(HOOC-COOH)的下列说法错误的是( )
A.9.0g草酸中共用电子对数目为0.9NA
B.9.0 g草酸被NaClO氧化生成CO2,转移的电子数为0.2 NA
C.9.0 g草酸溶于水,其中C2O42-和HC2O4-的微粒数之和为0.1NA
D.9.0g草酸受热完全分解为CO2、CO、H2O,标况下测得生成的气体体积为4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是化学学习与研究的常用方法,下列分类正确的是
A.Cl2O7、P2O5、SO3、CO2均属于酸性氧化物
B.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com