
| I1 | I2 | I3 | I4 | … | |
| 电离能(kJ/mol) | 738 | 1451 | 7733 | 10540 | … |

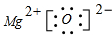 ,
,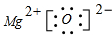 ;
;

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2015届江苏省徐州市高二上学期期末考试化学试卷(必修)(解析版) 题型:填空题
化学和环境保护、食品营养、材料应用等密切相关。
(1)防治环境污染、改善生态环境已成为全人类的共识。
①下列各项中,完成空气质量报告时不需要监测的是 (填字母)。
A.可吸入颗粒物的浓度
B.二氧化氮的浓度
C.二氧化碳的浓度
②下列做法中不利于改善环境质量的是 (填字母)。
A.将废旧电池进行深埋处理
B.充分利用太阳能等清洁能源
C.给汽车加装尾气催化净化装置
③工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是 (填字母)。
A.沉淀法 B.中和法 C.氧化还原法
(2)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①人体需要的营养素主要有糖类、 、蛋白质、无机盐、维生素和水。在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是 。
②下列物质中,具有解热镇痛疗效的是 (填字母)。
A.氨基酸 B.阿斯匹林 C.青霉素
③有些药片常用淀粉作为黏合剂,淀粉进入人体后在人体内酶的催化作用下逐步水解,最终转化为 (填物质的名称)。维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和 试剂共同完成。
(3))材料是人类社会发展的物质基础,材料科学的发展离不开化学。
①陶瓷、水泥和普通玻璃都是生活中最常见的材料,它们属于 (填字母)。
A.金属材料 B.无机非金属材料 C.有机高分子材料
制造普通玻璃时,需要的主要原料有纯碱、石灰石和 (填化学式)。
②钢铁制品在潮湿的空气中发生 (填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因。硬铝(一种铝合金)是制造飞机和宇宙飞船的理想材料,和纯铝相比,硬铝的强度 (填“低”、“高”或“无法确定”),具有较强的抗腐蚀能力。
③在尼龙、棉花、涤纶这三种物质中,属于天然纤维的是 。橡胶是制造轮胎的重要原料,天然橡胶通过 (填“硫化”、“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。“白色污染”已成为当今社会的一大公害,“白色污染”主要是 (填“废塑料制品”、“废橡胶制品”或“生活垃圾”)造成的。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市高三上学期期中考试化学试卷(解析版) 题型:填空题
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等
|
|
|
J |
|
|
|
|
|
|
|
R |
M的气态原子逐个失去1~ 4个电子所需能量(电离能)如下表所示,
|
|
I1 |
I2 |
I3 |
I4 |
…… |
|
电离能(kJ/mol) |
578 |
1817 |
2745 |
11578 |
…… |
(1)M的电子排布式为________;元素T在周期表中的位置为________。
(2)J和氢能形成多种化合物,其中分子成直线型的,且相对分子质量最小的物质的结构式为________。
(3)M和T形成的化合物在潮湿的空气中冒白雾,反应的化学方程式为_________________。
(4)由J、R形成的液态化合物JR2 0.2 mol在O2中完全燃烧,生成两种气态氧化物,298 K时放出热量215 kJ。该反应的热化学方程式为________。
(5)能源材料已成为当今科学研究的热点。氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。继C60后,科学家又合成了Si60、N60,下列有关说法正确的是_______(填序号)。
a. C60、Si60、N60都属于新型化合物
b. C60、Si60、N60互为同分异构体
c. 已知N60结构与C60相似,由于N-N键能小于N≡N,故N60的稳定性弱于N2
d. 已知金刚石中C-C键长154pm,C60中C-C键长145~140pm,故C60熔点高于金刚石
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com