
| A£®Į× | B£®Įņ | C£®Ć¾ | D£®Ķ |
 Fe(OH)3+3H+CaCO3+2H+====Ca2++CO2”ü+H2O£Ø2£©C£Ø3£©¢ŁFe(OH)30.06mol¢Ś0£¼x”Ü0.6
Fe(OH)3+3H+CaCO3+2H+====Ca2++CO2”ü+H2O£Ø2£©C£Ø3£©¢ŁFe(OH)30.06mol¢Ś0£¼x”Ü0.6 Fe(OH)3+3H+2H++CaCO3====Ca2++H2O+CO2”üĖłŅŌ£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬ČÜŅŗŃÕÉ«¼ÓÉī£¬²śÉśŗģŗÖÉ«³Įµķ£¬Ķ¬Ź±Éś³ÉCO2”£
Fe(OH)3+3H+2H++CaCO3====Ca2++H2O+CO2”üĖłŅŌ£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬ČÜŅŗŃÕÉ«¼ÓÉī£¬²śÉśŗģŗÖÉ«³Įµķ£¬Ķ¬Ź±Éś³ÉCO2”£ ,ĪŽ³Įµķ”£
,ĪŽ³Įµķ”£ £¬øł¾ŻµēŗÉŹŲŗćµĆ£ŗ
£¬øł¾ŻµēŗÉŹŲŗćµĆ£ŗ


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓÉ0.1mol”¤L-1µÄCH3COOHČÜŅŗÓė0.1mol”¤L-1µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ¶ų³É |
| B£®ÓÉ10mLpH=3µÄCH3COOHČÜŅŗÓė1mLpH=11µÄNaOHČÜŅŗ»ģŗĻ¶ų³É |
| C£®ÓÉ0.1mol”¤L-1µÄCH3COONaČÜŅŗÓė0.1mol”¤L-1µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ¶ų³É |
| D£®ÓÉ0.1mol”¤L-1µÄCH3COONaČÜŅŗÓė0.1mol”¤L-1µÄCH3COOHČÜŅŗµČĢå»ż»ģŗĻ¶ų³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

 H++
H++ £¬ÓūŹ¹ČÜŅŗÖŠc(
£¬ÓūŹ¹ČÜŅŗÖŠc( )”¢c(H+)”¢c(
)”¢c(H+)”¢c( )¶¼¼õŠ”£¬æÉŅŌ²ÉČ”µÄ·½·ØŹĒ()
)¶¼¼õŠ”£¬æÉŅŌ²ÉČ”µÄ·½·ØŹĒ()| A£®¼ÓNaOH | B£®¼ÓŃĪĖį | C£®¼ÓŹÆ»ŅĖ® | D£®¼ÓĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®0.1mol”¤L-1µÄFeCl3ČÜŅŗ | B£®0.1mol”¤L-1µÄAlCl3ČÜŅŗ |
| C£®0.05mol”¤L-1µÄNa2SČÜŅŗ | D£®0.05mol”¤L-1µÄAl2£ØSO4£©3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 )ĻąĶ¬µÄĻĀĮŠČÜŅŗ¢ŁNH4Cl¢Ś(NH4)2SO4?¢ŪNH4HSO4?¢ÜNH4HCO3,ĘäĪļÖŹµÄĮæÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ£Ø£©
)ĻąĶ¬µÄĻĀĮŠČÜŅŗ¢ŁNH4Cl¢Ś(NH4)2SO4?¢ŪNH4HSO4?¢ÜNH4HCO3,ĘäĪļÖŹµÄĮæÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ£Ø£©| A£®¢Ś¢Ü¢Ł¢Ū |
| B£®¢Ś¢Ū¢Ł¢Ü |
| C£®¢Ł¢Ü¢Ū¢Ś |
| D£®¢Ü¢Ł¢Ū¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
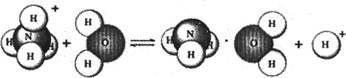
A£®“ęŌŚNH3”¤H2O£¬Ęä½į¹¹Ź½ĪŖ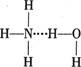 | B£®“ęŌŚNH4+£¬Ęäµē×ÓŹ½ĪŖ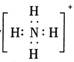 |
C£®“ęŌŚH3O+£¬Ęä½į¹¹Ź½ĪŖ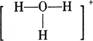 | D£®“ęŌŚOH££¬Ęäµē×ÓŹ½ĪŖ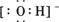 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Į½ÕßĻąµČ | B£®Ē°ÕߏĒŗóÕßµÄ105±¶ |
| C£®ŗóÕߏĒĒ°ÕßµÄ104±¶”””””” | D£®ĪŽ·Ø±Č½Ļ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com