
【题目】长征2号火箭承担运载“神六”的使命,氕化锂、氘化锂、氚化锂可以作为启动长征2号(CZ2F)火箭的优良炸药。下列说法正确的是
A. LiH、LiD、LiT的摩尔质量之比为1∶2∶3 B. 它们都是强还原剂
C. H、D、T之间互称为同素异形体 D. 它们都是强氧化剂
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】【化学——选修物质结构与性质】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在 对自旋相反的电子,基态氮原子的价层电子排布图为_________________________。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为 ,其中氧原子的杂化方式为 。
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= 。CO与N2结构相似,CO分子内σ键与π键个数之比为 。
(4)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是 。
(5)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释H2SeO4比H2SeO3酸性强的原因: ;
(6)已知Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
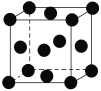
(7)用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,Cu的原子半径为________cm(阿伏加德罗常数为NA,只要求列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知某溶液中只存在OH-、H+、NH4+、CL-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
⑴若溶液中只有一种溶质,则该溶质是_________________。
⑵若四种离子的关系符合③,则溶质为___________;若四种离子的关系符合④,则溶质为________。
⑶将pH相同的NH4Cl溶液稀释相同的倍数,下面图像正确的是(填图像序号)______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.1molH2的质量只有在标准状况下才约为2g
B.标准状况下,22.4L氖气含有的原子数为2NA
C.标准状况下,22.4LH2O含有的分子数为NA
D.同温同压下,相同体积的气体单质含有的原子数目不一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”实施的是
A.推广使用燃煤脱硫技术,减少SO2污染
B.实施绿化工程,防治扬尘污染
C.加快清洁能源的开发利用
D.加大石油、煤炭的开发速度,提倡使用化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g)ΔH,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g)ΔH,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:

①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(N2)=________mol/(Lmin);计算该反应的平衡常数K=___________。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是________(填字母代号)。
A.加入合适的催化剂
B.适当缩小容器的体积
C.通入一定量的NO
D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率________(填“升高”或“降低”),ΔH________0(填“>”或“<”).
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1=-49.1kJ/mol
CH3OH(g)+H2O(g)△H1=-49.1kJ/mol
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g)△H2=-24.5kJ/mol
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式__________________。
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Al、Mg混合物加入到足量的盐酸中,充分反应后得到标准状况下的氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气6.72L.
(1)当混合物与盐酸反应时,转移电子总物质的质量为______mol;
(2)求混合物中Al质量为 __________g Mg的质量为_________g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com