
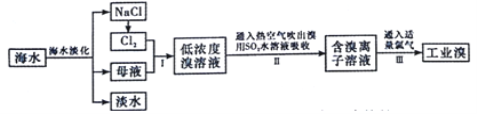
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图:
(1)除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是______.
A.NaOH溶液→碳酸钠溶液→氯化钡溶液→过滤后加盐酸
B.氯化钡溶液→氢氧化钠溶液→碳酸钠溶液→过滤后加盐酸
C.NaOH溶液→氯化钡溶液→碳酸钠溶液→过滤后加盐酸
D.碳酸钠溶液→氢氧化钠溶液→氯化钡溶液→过滤后加盐酸
(2)写出Ⅱ中发生反应的离子方程式:______.
(3)从理论上考虑,下列物质也能吸收的是______
A.NaOH![]()
![]()
![]()
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是______.
(5)已知某溶液中Cl-、Br-、I-的物质的量之比为3:4:5,现欲使溶液中的Cl-、Br-、I-的物质的量之比变成3:2:1,那么要通入氯气的物质的量是原溶液中I-的物质的量是______
A.1/2B.1/10C.3/10D.1/5
【答案】BCBr2+SO2+2H2O=4H++2Br-+SO42-ABCCl2>Br2>SO2C
【解析】
海水淡化得到淡水和氯化钠,电解氯化钠溶液生成氯气,氯气通入母液中发生反应得到低浓度的溴单质溶液,通入热空气吹出后用二氧化硫水溶液吸收得到含HBr和硫酸的溶液,通入适量氯气氧化得到溴单质,富集溴,蒸馏得到工业溴,(1)除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,盐酸要放在最后,以除去过量的氢氧化钠和碳酸钠,应该先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子,即:加入的碳酸钠溶液必须放在加入氯化钡溶液之后;(2)Ⅱ中发生反应是溴单质氧化二氧化硫生成硫酸;(3)溴单质和氢氧化钠溶液反应,或和还原性的物质发生氧化还原反应;(4)氧化还原反应方程式中:氧化性:氧化剂大于氧化产物,氧化剂大于还原剂;(5)已知还原性I->Br->Cl-,反应后I-有剩余,说明Br-浓度没有变化,通入的Cl2只与I-发生反应,根据反应的方程式2I-+Cl2=2Cl-+I2计算。
(1)要先除SO42-离子,然后再除Ca2+离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加NaOH除去Mg2+离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,只要将三种离子除完了,然后过滤即可,最后加盐酸除去过量的氢氧根离子、碳酸根离子,所以正确的操作顺序为:A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸,最后加入的氯化钡溶液中钡离子不能除去,选项A错误;B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,选项B正确;C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸,选项C正确;D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸,顺序中加入的氯化钡溶液中钡离子无法除去,选项D错误;答案选BC;
(2)Ⅱ中发生反应是溴单质氧化二氧化硫生成硫酸,反应的离子方程式为:Br2+SO2+2H2O=4H++2Br-+SO42-;
(3)A.NaOH溶液和溴单质反应生成溴化钠、次溴酸钠和水,可以吸收,选项A正确;B.FeCl2 溶液具有还原性,可以被溴单质氧化为氯化铁,可以吸收溴单质,选项B正确;C.Na2SO3 溶液具有还原性,可以被溴单质氧化,能吸收溴单质,选项C正确;D.H2O和溴单质反应微弱,不能充分吸收溴单质,选项D错误;答案选ABC;
(4)Cl2+2Br-=Br2+2Cl-,根据氧化还原反应中氧化性:氧化剂大于氧化产物,所以氧化性:Cl2>Br2;Br2+SO2 +2H2O=H2SO4 +2HBr,根据氧化还原反应中氧化性:氧化剂大于还原剂,所以氧化性:Br2>SO2;故答案为:Cl2>Br2>SO2;
(5)已知还原性I->Br->Cl-,反应后I-有剩余,说明Br-浓度没有变化,通入的Cl2只与I-发生反应,设原溶液中含有3molCl-,4molBr-,5molI-,通入Cl2后,它们的物质的量之比变为3:2:1,即6:4:2,此时氯离子增大3mol,碘离子减少3mol,溴离子不变,则各离子物质的量分别为:6molCl-,4molBr-,2molI-,Cl-增加3mol,I-离子减少3mol,Br-不变,则需1.5molCl2,则通入的Cl2物质的量是原溶液中I-物质的量的 ![]() =
=![]() ,答案选C。
,答案选C。


科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数时,不能作为达到平衡标志的是
pC(g)+qD(g),当m、n、p、q为任意整数时,不能作为达到平衡标志的是
A. 体系的压强不再改变B. 体系的温度不再改变
C. 各组分的浓度不再改变D. 各组分的质量分数不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是一种香料,可用如下路线合成:

已知:①双键在链端的烯烃发生硼氢化-氧化反应,生成的醇羟基在链端:

②![]()
③A、B发生同一反应类型有机物都只生成C
④核磁共振氢谱显示E分子中有两种氢原子,F为芳香族化合物。
请回答下列问题:
(1)原料C4H10的名称是 _______________(用系统命名法);
(2)写出反应A→C的反应试剂和条件:____________________;
(3)F与新制Cu(OH)2反应的化学方程式 _______________________;
(4)D +G →M反应的化学方程式_________________________;
(5)写出N、M的结构简式 _________________、_________________;
(6)写出与G具有相同官能团的G的所有芳香类同分异构体(不包括G本身)的结构简式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向60 mL Na2SO4溶液中加入BaCl2溶液,有关数据见下表:
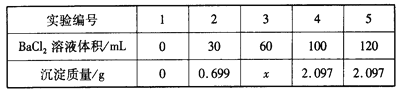
下列有关说法不正确的是
A. 混合前,BaCl2溶液的物质的量浓度为0.10 mol·L-1
B. 混合前,Na2SO4溶液的物质的量浓度为0.15 mol·L-1
C. 3号实验中沉淀的质量x为1.398 g
D. 完全沉淀60 mL Na2SO4溶液消耗BaCl2溶液的体积为80 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组设计用含氯的有机物A合成棉织物免烫抗皱整理剂M的路线如下(部分反应试剂和条件未注明):
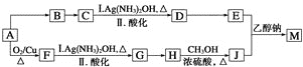
已知:①E的分子式为C5H8O4,能发生水解反应,核磁共振氢谱显示E分子内有2种不同化学环境的氢原子,其个数比为3∶1;
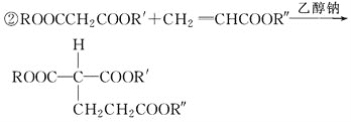
(R、R′、R″代表相同或不相同的烃基)。
(1)A分子中的含氧官能团的名称是________________。
(2)D→E反应的化学方程式是____________。
(3)A→B反应所需的试剂是________________。
(4)G→H反应的化学方程式是____________。
(5)已知1 mol E与2 mol J反应生成1 mol M,则M的结构简式是________。
(6)E的同分异构体有下列性质:①能与NaHCO3反应生成CO2;②能发生水解反应,且水解产物之一能发生银镜反应,则该同分异构体共有________种,其中任意1种的结构简式是________。
(7)J可合成高分子化合物,该高分子化合物的结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯元素及氯气的叙述中,正确的是( )
A.干燥的氯气可以贮存在钢瓶中
B.氯元素在自然界中既有化合态存在,也有游离态存在
C.氯气难溶于水,可直接用排水法收集氯气
D.氯水、液氯是状态不同的同一种物质,均属于纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为测定某烧碱样品中![]() 的质量分数,进行如下实验:(已知该样品中含有少量不与酸作用的杂质)
的质量分数,进行如下实验:(已知该样品中含有少量不与酸作用的杂质)
A.在250![]() 的容量瓶中定容,配制成250
的容量瓶中定容,配制成250![]() 烧碱溶液;
烧碱溶液;
B.用碱式滴定管移取25.00![]() 烧碱溶液于锥形瓶中,并滴几滴甲基橙指示剂;
烧碱溶液于锥形瓶中,并滴几滴甲基橙指示剂;
C.在天平上准确称取20.5![]() 烧碱样品,在烧杯中用蒸馏水溶解;
烧碱样品,在烧杯中用蒸馏水溶解;
D.将物质的量浓度为1.00![]() 的标准硫酸溶液装入酸式滴定管中,调节液面,记下开始时的读数;
的标准硫酸溶液装入酸式滴定管中,调节液面,记下开始时的读数;
E.在锥形瓶下垫一张白纸,滴定至溶液变为橙色为止,记下读数。
试填空:
(1)正确操作步骤的顺序是________→________→________→________→________。(用字母填空)
(2)观察滴定管液面的读数时应注意什么问题?
_____________________________________________________________________。
(3)![]() 步操作中的锥形瓶下垫一张白纸的作用是__________________________________________。
步操作中的锥形瓶下垫一张白纸的作用是__________________________________________。
(4)下列操作中可能使所测![]() 溶液的质量分数偏低的是________。
溶液的质量分数偏低的是________。
a.![]() 步操作中未将溶液冷却至室温就转移到容量瓶中定容
步操作中未将溶液冷却至室温就转移到容量瓶中定容
b.![]() 步操作中,称量药品时,砝码放在左盘,
步操作中,称量药品时,砝码放在左盘,![]() 放在右盘
放在右盘
c.![]() 步操作中酸式滴定管在装入标准
步操作中酸式滴定管在装入标准![]() 溶液前未用标准液润洗
溶液前未用标准液润洗
d.滴定过程中,读取硫酸溶液体积时,开始时仰视读数,结束时俯视读数

(5)硫酸的初读数和末读数如图所示。未读数为________![]() ,初读数为________
,初读数为________![]() ,用量为________
,用量为________![]() 。按滴定所得数据计算烧碱样品中
。按滴定所得数据计算烧碱样品中![]() 的质量分数为________。
的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com