
 如图所示,已知:
如图所示,已知:
| ||
| 高温高压 |
| ||
| 高温高压 |
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
| A | B | C | D | |
| 电极与溶液 | Zn、C硫酸 | Cu、Ag硝酸银 | Zn、Cu蔗糖 | Mg、Al氢氧化钠 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 加入试剂 | 离子方程式 |
| NaCl(NaHCO3) | HCl | |
| K2CO3(KOH) | CO2 | |
| NaHCO3(Na2CO3) | CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
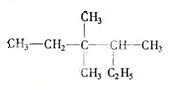 按系统命名法命名为
按系统命名法命名为 ,在A的同分异构体中,能催化氧化
,在A的同分异构体中,能催化氧化查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、研制高性能的耐磨轮胎,可减少细颗粒物(PM2.5)的产生 |
| B、将聚乙烯等塑料垃圾深埋或倾入海中 |
| C、利用微生物发酵技术,将植物秸秆、动物粪便等制成沼气 |
| D、利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯塑料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
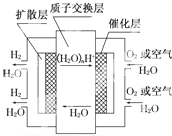
| A、正极反应为:O2+4H++4e-═2H2O |
| B、负极反应为:2H2-4e-═4H+ |
| C、导电离子为质子,且在电池内部由正极定向移动至负极 |
| D、总反应式为:2H2+O2═2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com