
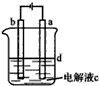
 ����Fe��OH��2���ױ�����������ʵ�������������������Һ���ռӦ�Ƶİ�ɫ������Fe��OH��2������Ӧ����ͼ��ʾ�ĵ��ʵ����Ƶð�ɫ����Fe��OH��2���������缫�IJ��Ϸֱ�Ϊʯī����������˵����ȷ���ǣ�������
����Fe��OH��2���ױ�����������ʵ�������������������Һ���ռӦ�Ƶİ�ɫ������Fe��OH��2������Ӧ����ͼ��ʾ�ĵ��ʵ����Ƶð�ɫ����Fe��OH��2���������缫�IJ��Ϸֱ�Ϊʯī����������˵����ȷ���ǣ�������| A��a�缫�����ĵ缫��Ӧ��4OH--4e-=O2��+2H2O |
| B��Ϊ���ڽ϶�ʱ���ڿ�����ɫ���������ʵ��Ӵ��ѹ |
| C��c�������Ȼ�����Һ��d���������Ȼ�̼ |
| D��Ϊ���ڽ϶�ʱ���ڿ�����ɫ���������Ծ��ҵؽ�����Һ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ɰ�ɫ���� |
| B���������ɺ��ɫ���� |
| C�����ճ��ֻ���ɫ���� |
| D���ޱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+Ũ�ȼ�С��HClOŨ�ȼ�С |
| B��H+Ũ������HClOŨ������ |
| C��H+Ũ������HClOŨ�ȼ�С |
| D��H+Ũ�ȼ�С��HClOŨ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A����Ӧ���ʦ�����X��=
| ||
| B�������¶ȣ���Ӧ������ֵ��� | ||
| C����Ӧ�ﵽ�����ʱ������X����Ӧ�ġ�H���� | ||
| D����һ���������������з���m molX��n mol Y����ַ�Ӧ����Q kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2Na+2H2O=2NaOH+H2�� |
| B��CaO+H2O=Ca��OH��2 |
| C��2F2+2H2O=4HF+O2 |
| D��Cl2+H2O=HCl+HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��FeS+2HCl=FeCl2+H2S�� |
| B��Fe+H2SO4=FeSO4+H2�� |
| C��FeO+2HCl=FeCl2+H2O |
| D��2FeCl3+Cu=2FeCl2+CuCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol NH4+ ����������Ϊ10NA |
| B��10 g��������ԭ����ԼΪ6.02��1023 |
| C��22.4 L SO2�����ķ�����ΪNA |
| D�����³�ѹ�£�32 g O2����ԭ����Ϊ2NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com