
����Ŀ������������(NOSO4H)��Ҫ����Ⱦ�ϡ�ҽҩ�ȹ�ҵ��ʵ��������ͼװ��(�г�װ����)��ȡ������NOSO4H���������Ʒ���ȡ���֪��NOSO4H��ˮˮ�⣬������Ũ��������ֽ⡣

��1������װ��A��ȡSO2�����������˵��Լ���_____(��������ĸ���)
A��Na2SO3�����20%���� B��Na2SO3�����20%����
C��Na2SO3�����70%���� D��Na2SO3�����18.4mol/L����
��2��װ��B��ŨHNO3��SO2��ŨH2SO4�����·�Ӧ�Ƶ�NOSO4H��
��Ϊ�˿���ͨ��SO2�����ʣ����Բ�ȡ�Ĵ�ʩ��_______��
�ڸ÷�Ӧ����ά����ϵ�¶Ȳ�����20�档���¶ȹ��ߣ����ʽ��͵Ŀ���ԭ����____��
�ۿ�ʼ��Ӧ����������������NOSO4H���¶ȱ仯������Ӧ�������Լӿ죬��ԭ�������______��
��3����ʵ��װ�ô��ڿ��ܵ���NOSO4H�������͵�ȱ����______��
��4���ⶨNOSO4H�Ĵ���
ȷ��ȡ1.337 g��Ʒ����250 mL����ƿ�У�����0.1000mol/L��60.00 mL��KMnO4����Һ��10 mL 25%H2SO4��Һ��Ȼ��ҡ�ȡ���0.2500 mol/L�����Ʊ���Һ�ζ������IJ�������Һ�����Ϊ20.00 mL��
��֪��2KMnO4��5NOSO4H��2H2O��K2SO4��2MnSO4��5HNO3��2H2SO4
����ƽ��__MnO4-��___C2O42-��______��___Mn2+��____��__H2O
������������Ĵ���=___%(������������λ��Ч����)��
���𰸡�C ���ڷ�Һ©������������Ũ����ĵμ��ٶ� ŨHNO3�ֽ⡢�ӷ� ���ɵ�NOSO4H��Ϊ�÷�Ӧ�Ĵ��� C(��A)�е�ˮ���������B��ʹ��Ʒ����ˮ�� 2 5 16H+ 2 10CO2�� 8 95
��������
���������֪����װ��B������ŨHNO3��SO2��ŨH2SO4�����·�Ӧ�Ƶ�NOSO4H������װ��A��ȡ������������װ��C���ն���Ķ�������ֹ��Ⱦ�������ݴ˷�����
��1����װ�����ڹ�Һ��ҺҺ��ϲ�������װ�á�Na2SO3��Һ��HNO3��Ӧʱ������������������Ʊ�������ԭΪһ��������ѡ��A�����ϣ�ʵ�����ƶ��������ԭ���ǻ���SO32-��H+�ķ�Ӧ����Ϊ���ɵ�SO2������ˮ�����Բ�����ϡ��������ȡ������������SO2���ݳ������������Ũ���ᣨ18.4mol/L�����������ǹ��ۻ����Ũ��Խ�ߣ�Խ��������������H+�����Բ��ʺ���̫Ũ����������ȡSO2��ѡ��B��ѡ��D�����ϣ�ѡ��C���ϣ���ѡC��
��2��װ��B��ŨHNO3��SO2��ŨH2SO4�����·�Ӧ�Ƶ�NOSO4H��
��Ϊ�˿���ͨ��SO2�����ʣ����Բ�ȡ�Ĵ�ʩ�ǵ��ڷ�Һ©������������Ũ����ĵμ��ٶȣ�
�ڸ÷�Ӧ����ά����ϵ�¶Ȳ�����20�档���¶ȹ��ߣ�ŨHNO3�ֽ⡢�ӷ������ʽ��ͣ�
�ۿ�ʼ��Ӧ����������������NOSO4H���¶ȱ仯�������ɵ�NOSO4H��Ϊ�÷�Ӧ�Ĵ�����ʹ��Ӧ�������Լӿ죻
��3����ʵ��װ�ô��ڿ��ܵ���NOSO4H�������͵�ȱ����C(��A)�е�ˮ���������B��ʹ��Ʒ����ˮ�⣻
(5)�ٷ�������MnO4����C2O42����������ԭ��Ӧ��MnO4����������������ԭ������Mn2+��C2O42������ԭ�����������ɳǶ�����̼����ϵ�ʧ�����غ�͵���غ�ɵõ�MnO4����C2O42�������ӷ�Ӧ����ʽΪ��2MnO4��+5C2O42��+16H+��2Mn2++10CO2��+8H2O��
�ڸ��������֪������KMnO4��Һ����NOSO4H��Ӧ�����ò�������Һ�ζ�ʣ������KMnO4��Һ����0.2500mol��L��1�����Ʊ���Һ�ζ�����KMnO4��Һ�����IJ�������Һ�����Ϊ20.00mL����֪ʣ���KMnO4�����ʵ���n1(MnO4��)=![]() n(C2O42��)=
n(C2O42��)=![]() ��0.2500mol��L��1��20.00��10-3L=2��10-3mol�����������������ĵ�KMnO4�����ʵ���n2(MnO4��)=0.1000mol��L��1��60.00��10-3L-2��10-3mol=4��10-3mol��n(NOSO4H)=5/2n2(MnO4��)=10-2mol������������Ĵ���=m(NOSO4H)/1.337g��100%=10-2mol��127 g��mol��1/1.337g��100%=95.0%��
��0.2500mol��L��1��20.00��10-3L=2��10-3mol�����������������ĵ�KMnO4�����ʵ���n2(MnO4��)=0.1000mol��L��1��60.00��10-3L-2��10-3mol=4��10-3mol��n(NOSO4H)=5/2n2(MnO4��)=10-2mol������������Ĵ���=m(NOSO4H)/1.337g��100%=10-2mol��127 g��mol��1/1.337g��100%=95.0%��


 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ�����þ��й���ǰ����
��1����ˮ�����ķ�����_____��ѡ��һ�ּ��ɣ���
��2���Ӻ�ˮ����ȡ�����Ҫ��������Ũ���ĺ�ˮ��ͨ�����������������������÷�Ӧ�����ӷ���ʽ��____��
��3����ͼ�ǴӺ�ˮ����ȡþ�ļ����̡�
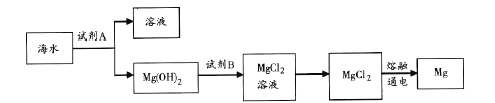
��ҵ�ϳ����ڳ���Mg2�����Լ�A ��������___��Mg(OH)2ת��ΪMgCl2 �����ӷ���ʽ��_______��
��4���������и�����I����ʽ���ڵĵ�Ԫ�ء�ʵ������ȡI2 ��;��������ʾ��
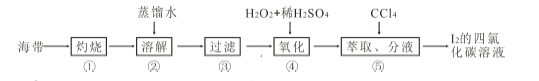
�����պ������ҽ�ʱ���õ���Ҫ����������_______������ڼ������һ���Ŀ����______________��
�� ���������Һ�м�H2O2 ��ϡH2SO4 ��Һ��д���÷�Ӧ�����ӷ���ʽ_______________����Ӧ�������ټ���CCl4 ����ȡ���������ã����Թ۲쵽CCl4 ���____________ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڻ���(Na2Te)�������л��ϳ��Լ������Ϸ�Ӧ�еĴ���������Ǧ��(��Ҫ�ɷ�ΪPbTe)�ʹ���(��CaCl2��MgCl2��һЩ�����Ρ���ɳ)Ϊԭ���Ʊ��ڻ��ƵĹ����������£�
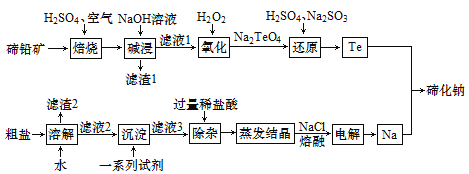
�ش��������⣺
(1)Na2TeO4��Te�Ļ��ϼ�Ϊ___��
(2)��������������һϵ���Լ�����������Щ�Լ����ΰ���_____(�ѧʽ)��NaOH��
(3)�������ᾧ��ʱ�õ�����Ҫ����������̨(����Ȧ)���ƾ��ơ�����ǯ��_____�ȡ�
(4)��֪��������������Ҫ��TeO2��ʽ���ڣ�����������Ӧ�Ļ�ѧ����ʽΪ____��
(5)����������������ԭ��������Ӧ����֪Na2TeO4��H2O2��Na2SO4��������ǿ������˳��Ϊ___������ԭ�������У���ԭ���������������ʵ�����Ϊ_______��
(6)���Ƶ�8.7kg�ڻ��ƣ������ϵ�������״�������������Ϊ______����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ǰ�߸պ��Ǻ����������� (����)
A. 2 mol H2O��Ħ��������1 mol H2O��Ħ������
B. 200 mL 1 mol��L-1�Ȼ�����Һ��c(Cl-)��100 mL 2 mol��L-1�Ȼ�����Һ��c(Cl-)
C. 64 g������������ԭ�����ͱ�״����22.4 Lһ����̼����ԭ����
D. 20% NaOH��Һ��NaOH�����ʵ���Ũ�Ⱥ�10% NaOH��Һ��NaOH�����ʵ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�صĵ��ʼ��仯������;�㷺��ij��ȤС�����Ʊ���������֤��һϵ�����ʡ�
I�����������ϣ�
�ٵ���ˮŨ�Ƚ�Сʱ����Һ��ɫ����ˮ����Ҳ�ʻ�ɫ
�����������(Na2S2O3)��Һ�ڹ�ҵ�Ͽ���Ϊ���ȼ�
II����������֤��
ʵ��װ����ͼ1��ʾ(ʡ�Լг�װ��)
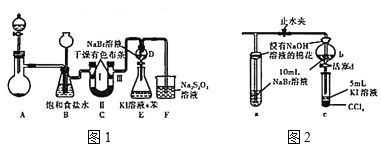
��1��װ��A��ʢ�Ź����Լ���������____�����ֱ���KMnO4��Ca(ClO)2��KClO3������������Ũ���ᷴӦ���������������ת�Ƶĵ�����֮��Ϊ____��
��2��װ��C��II�����ӵ��Լ�������____(��������ĸ���)
A����ʯ�� B��Ũ���� C������ D����ˮ�Ȼ���
��3��װ��B�������У���ȥ�����е��Ȼ��⡢______��_____��
��4��������Br2�Ļӷ�������F��Һ��Cl-��Ҫ���Լ���_______��
III����̽���ͷ�˼��
ͼһ�����װ��D��E��Ŀ���DZȽ��ȡ��塢��ķǽ����ԣ���ͬѧ��Ϊ����Ʋ��ܴﵽʵ��Ŀ�ġ������ͬѧ˼��������D��E��Fװ�ø�Ϊͼ2װ�ã�ʵ������������£�
�ٴ�ֹˮ�У�����ͨ���������ڵ�a��b�е���Һ����Ϊ��ɫʱ���н�ֹˮ�У�
�۵�a����Һ�ɻ�ɫ��Ϊ��ɫʱ��ֹͣͨ�������ܡ�
��5����Ʋ���۵�Ŀ����______��
��6��������Ϊ�ȡ��塢��ǽ����Եݱ�����ж����ݵ���_____(��������ĸ���)
A��Cl2��Br2��I2���۵� B��HCl��HBr��HI������
C��HCl��HBr��HI�����ȶ��� D��HCl��HBr��HI�Ļ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л������ʽΪC4H8���ݴ��Ʋ���ṹ�����ʲ����ܵ���
A. ������ϩ������ͬϵ��
B. һ�ȴ���ֻ��һ��
C. ��������CH4��C4H8���ֱ�����������ȫȼ�գ�CH4�ĺ�����С��C4H8
D. ���ӽṹ�м�����Ŀ������0��1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�ȷ��Ʊ�Fe3O4���������ܷ�ӦΪ��3Fe2++2S2O32-+O2+XOH- =Fe3O4+S4O62-+2H2O������˵����ȷ���ǣ� ��
A. ��Ԫ�ر���������Ԫ�ر���ԭ
B. Fe2+��S2O32- ���ǻ�ԭ��
C. X=2
D. ÿ����1mol Fe3O4����ת�Ƶ�����2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽ��Ӧʵ��Ŀ�ĵ���
ѡ�� | ʵ��Ŀ�� | ʵ����� |
A | ̽��I-��Fe2+�Ļ�ԭ��ǿ�� | ��FeCl3ϡ��Һ�����μ���KI��Һ������ |
B | ̽��HPO42-��ˮ��Һ�еĵ���̶���ˮ��̶ȵ���Դ�С | �ⶨ0.1 mol��L-1NaH2PO4��Һ��pH |
C | ����0.1 mol��L-1�ڱ����������( | ��ȡ5.1 g�ڱ�������������ձ���,������������ˮ�ܽ�,ת����500 mL����ƿ�ж��� |
D | �Ƚ�CaCO3��CaSO4��Ksp��С | �����ʯ��ˮ�е���0.1 mol��L-1Na2CO3��Һ�������г�������,�ٵμ�0.1 mol��L-1Na2SO4��Һ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Σ�3PbO��PbSO4��H2O����Է�������Ϊ990��������������ϩ�����ȶ����� ������ˮ����200.0tǦ�ࣨ��Ҫ�ɷ�ΪPbO��Pb��PbSO4�ȣ�Ϊԭ���Ʊ����εĹ�����������ͼ��ʾ��

��֪��Ksp(PbSO4)=1.82��l0-8��Ksp(PbCO3)=l.46��l0-13��
�ش��������⣺
��1����Na2CO3��Һת����Ŀ����_________.
��2������ʱ,��ֱ��ʹ��H2SO4��Һ��ԭ�������________;Ǧ�����������ܹ����з�����Ӧ�����ӷ���ʽΪ__________.
��3�������п�ѭ�����õ�������_________��ϴ�Ӳ���ʱ����������Ƿ�ϴ�Ӹɾ��ķ�����________��
��4��������ת����ƽ��ʱ����Һl��c(SO42-)��c(CO32-)�ı�ֵΪ_____________��
��5�� 50-60��ʱ�ϳ����εĻ�ѧ����ʽΪ______�����õ��������������99.0t������Ǧ���е�ǦԪ����80��ת��Ϊ���Σ���Ǧ����ǦԪ�ص���������Ϊ_________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com