
下列说法不正确的是
A.太阳能电池板中有高纯硅单质,光导纤维的主要成分也是硅
B.分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法
C.核磁共振谱、红外光谱、紫外光谱和质谱法的综合运用,可用于分析有机物的结构
D.绿色荧光蛋白在研究癌症发病机制的过程中应用突出,在酸性或碱性条件下可能会失去发光功能
A
【解析】
试题分析:A. 太阳能电池板中有高纯硅单质,光导纤维的主要成分是二氧化硅。错误。B. 分类方法可以为我们的化学学习节约大量的时间;统计方法可以使我们掌握物质的反应规律;定量研究可以使我们掌握物质的性质与反应物的量的关系;实验方法是我们学习掌握第一手资料,提高学习化学的兴趣,加深对知识的理解和掌握;模型化方法可以使我们在在物质的分子结构的认识上有直观、形象的认识。因此这些方法都是化学研究的常用方法。正确。C.在有机物中通常存在同分异构体现象。为了认识物质的结构,通常采用 核磁共振谱、红外光谱、紫外光谱和质谱法的综合运用的方法。正确。D. 绿色荧光蛋白在研究癌症发病机制的过程中应用突出,蛋白质在酸性或碱性条件下会发生水解反应最终得到氨基酸,因此可能会失去发光功能。正确。
考点:考查物质的性质及应用和研究方法的知识。


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源:2013-2014湖北省四校下学期期中考试高一化学试卷(解析版) 题型:填空题
(14分)X、Y、Z、D、E、W是原子序数依次递增的短周期主族元素。
(1)Y元素的气态氢化物与其最高价氧化物对应水化物能发生化合反应生成一种盐,该反应的化学方程式为________________________________;Y与氢原子按个数比1:2形成的含18个电子的化合物的电子式为________________。
(2)X、E同主族,纯净的单质E可用于制太阳能电池,则X在周期表中的位置是________________;X与E作电极,同NaOH溶液可构成原电池,则该电池负极的电极反应式为:______________ 。
(3)常温常压下,W的单质为气体,且常用于自来水的消毒,W的一种氧化物W2O是酸性氧化物,W2O与水反应的方程式为______________ __________________,W2O的结构式为_____________。
(4)Z、D、E、W同周期,D的简单离子半径是同周期简单离子中半径最小的, D的单质与Z的最高价氧化物对应水化物反应的离子方程式为________________________________。
(5)(XY)2与W2性质相似,则(XY)2分子中含有的化学键有_____________________ (填“离子键”、“极性键”或“非极性键”);(XY)2的制备原理同实验室制取W2类似,在酸性条件下用MnO2氧化对应的阴离子得到。写出制取(XY)2的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省绍兴市柯桥区高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂,广泛用于纺织工业。
其制备过程如下:
①把甲酸(HCOOH)和足量的NaOH溶液混合;
②用Na2SO3固体和某酸反应制备SO2气体;
③在一定温度下,将足量的SO2气体通入①的溶液中,即有保险粉生成,同时生成一种气体。
(1)写出NaOH的电子式
(2)制备SO2时所选用的酸,你认为下列最适宜选用的是
A.浓盐酸 B.质量分数为70%的H2SO4
C.稀硝酸 D.质量分数为10%的稀硫酸
(3)制备保险粉的化学方程式可表示为
(4)保险粉可以用于除去废水中的重铬酸根离子(Cr2O72-被转化为Cr3+),这是目前除去酸性废水中铬离子的有效方法之一,则每消耗0.1mol保险粉,理论上可以除去Cr2O72-的物质的量为 mol。
(5)保险粉不稳定,容易分解生成甲、 乙、 丙三种化合物。若将甲、乙两种物质分别配成溶液,在甲溶液中加入稀硫酸,则有淡黄色沉淀和气体丙产生;乙溶液中加入BaCl2溶液和稀盐酸,有气体丙产生,但无白色沉淀。在甲溶液中加入稀硫酸后所发生反应的离子方程式为 保险粉分解的化学方程式为
(6)保险粉在空气中容易吸收氧气而发生氧化。其方程式为:
①2Na2S2O4+O2+H2O=4NaHSO3 或 ②2Na2S2O4+O2+H2O=4NaHSO3+NaHSO4
请设计实验证明氧化时发生的是②的反应。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高三下学期联考理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.金属汞一旦洒落,必须尽可能收集起来,放在水中保存以防挥发;并将硫磺粉撒在洒落的地方,使金属汞转变成不挥发的硫化汞
B.胶状沉淀和颗粒太小的沉淀不能用抽滤的原因是在快速过滤时沉淀易透过滤纸
C.用移液管吸取溶液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管
D.将水杨酸、乙酸酐和浓硫酸在锥形瓶中混合后,水浴加热,一段时间后取出锥形瓶,为使阿司匹林完全结晶需向锥形瓶中加适量的水,并将锥形瓶置于冰水浴中
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省湖州市高三二模理综化学试卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,实验装置如图1所示。电解过程中的实验数据如图2所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标况)。则下列说法中正确的是


A.电解过程中,b电极表面先有红色物质析出,然后才有气泡产生
B.从开始到Q点时收集到的混合气体的平均相对分子质量为17
C.曲线OP 段表示H2和O2混合气体的体积变化,曲线PQ段表示O2的体积变化
D.a电极上发生反应的方程式为:2H+ + 2e- = H2↑和4OH-–4 e-=2H2O+ O2↑
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省温州市业水平考试适应性测试化学试卷(解析版) 题型:推断题
(4分)已知:A是石油裂解气的主要成分,现以A为主要原料合成乙酸乙酯,其合成路线如图所示。请回答下列问题:
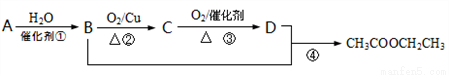
(1) B物质中官能团的名称____________。
(2) 写出反应③的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省温州市业水平考试适应性测试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数。下列说法正确的是
A.标准状况下,22.4 L 苯中含有的苯分子数是NA
B.标准状况下,1mol氦气中含有的核外电子数为4NA
C.常温常压下,15g乙烷分子中含有的碳氢键数目为3 NA
D.常温常压下,0.10 mol·L-1CH3COOH溶液中含有的H+数小于0.1NA
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省温州市业水平考试适应性测试化学试卷(解析版) 题型:选择题
下列关于液氯的说法中,不正确的是
A. 液氯属于混合物 B.液氯呈黄绿色
C. 液氯是一种有色、有味、有毒的液体 D.液氯能使湿润的红色布条褪色
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高一下学期期中化学试卷(解析版) 题型:选择题
已知CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-Q1 ①
2H2(g)+O2(g) ===2H2O(g) ΔH=-Q2 ②
H2O(g) ===H2O(l) ΔH=-Q3 ③
常温下,取体积比为4∶1的甲烷和H2的混合气体112 L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为 ( )
A.4Q1+0.5Q2+9Q3 B.4Q1+0.5Q2 C.4Q1+Q2+10Q3 D.4Q1+2Q2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com