
| A、431 kJ/mol |
| B、945.6 kJ/mol |
| C、649 kJ/mol |
| D、869 kJ/mol |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、推广燃煤脱硫技术,减少 SO2气体对大气的污染 |
| B、为改善食物的色、香、味并防止变质,可加入大量食品添加剂 |
| C、开发太阳能、潮汐能、风能等新能源,减少温室气体的排放 |
| D、用可降解的“玉米塑料”制作一次性饭盒,减少“白色污染” |
查看答案和解析>>
科目:高中化学 来源: 题型:
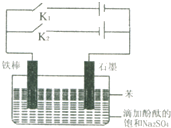 同学用电解原理设计一个观察Fe(OH)2沉淀和Fe(OH)2被氧化的实验装置.如图所示,有关该装置的说法正确的是( )
同学用电解原理设计一个观察Fe(OH)2沉淀和Fe(OH)2被氧化的实验装置.如图所示,有关该装置的说法正确的是( )| A、断开K2,接通K1,铁棒和石墨棒上都放出大量气泡,两电极附近溶液颜色均无变化 |
| B、断开K2,接通K1,仅石墨捧上放出大量气泡,石墨电极附近溶液变红,一段时间后水槽中可见白色沉淀生成且保持较长时间不变色 |
| C、断开K2,接通K1,一段时间后再断开K1,接通K2,由于苯层的保护作用,白色沉淀仍能长时间保持不变色 |
| D、若先断开K1,接通K2,铁棒和石墨棒上都放出大量气泡,石墨电极附近溶液变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g) | ||
B、C2H2(g)+
| ||
C、C2H2(g)+
| ||
D、C2H2(g)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①>② | B、①<② |
| C、①=② | D、不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量浓度为0.5 mol/L的MgCl2溶液,含有Cl- 个数为NA |
| B、V mL硫酸铁溶液中含有mg SO42-,则Fe3+的物质的量浓度为6.94m/V mol?L-1 |
| C、将58.5 g NaCl溶解于1 L水中配成溶液,所得溶液的物质的量浓度为1 mol?L-1 |
| D、用36.5%的浓盐酸(密度为1.25g?cm-3)配制成浓度为0.1mol?L-1的稀盐酸240ml,所需浓盐酸的体积为1.9mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
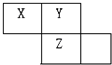 X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )| A、Z的氧化物对应的水化物一定是一种强酸 |
| B、原子半径大小顺序是X>Y>Z |
| C、Z单质与Fe反应形成的化合物中,铁元素显+3价 |
| D、Y的单质比Z的单质更易与氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(NH4)2SO4溶于水:(NH4)2SO4═2NH4++SO42- |
| B、H3PO4溶于水:H3PO4═3H++PO43- |
| C、HF溶于水:HF?H++F- |
| D、NaHS溶于水:NaHS═Na++HS-,HS-?H++S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com