
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
分析 根据分子式为C11H16的不饱和度为4,芳香烃中含有苯环,苯环的不饱和度为4,所以含有1个苯环,侧链为烷基,烷基的组成为-C5H11,先写出戊烷的同分异构体有正戊烷、异戊烷和新戊烷,然后用苯环确定戊烷上的取代位置,则可以写出其同分异构体.
解答 解:有分子式为C11H16的不饱和度为4,芳香烃中含有苯环,苯环的不饱和度为4,所以含有1个苯环,侧链为烷基,烷基的组成为-C5H11,
戊烷的同分异构体有:①正戊烷CH3CH2CH2CH2CH3、②异戊烷CH3CH2CH(CH3)CH3 ③新戊烷 C(CH3)4,
其中①正戊烷分子中氢原子被苯环取代所得的同分异构体有三种,分别为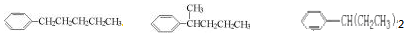
②异戊烷中氢原子被苯环取代的同分异构体有四种:
③新戊烷中氢原子被苯环确定的同分异构体有1种,其结构简式为 ,
,
所以C11H16的含有一个苯环且只有一个侧链同分异构体共有8种,
故选C.
点评 本题考查了同分异构体的书写,题目难度中等,明确同分异构体的书写原则为解答关键,试题侧重考查学生解题思维与解题方法,注意根据换元法进行分析判断.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:解答题
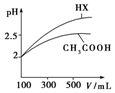 25℃时部分弱电解质的电离平衡常数数据如表所示:
25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
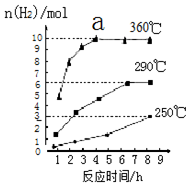 磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答:
磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷跟氯气发生取代反应 | B. | 乙烯跟氯气发生加成反应 | ||
| C. | 乙烷跟氯化氢混合 | D. | 乙烯跟氯化氢发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
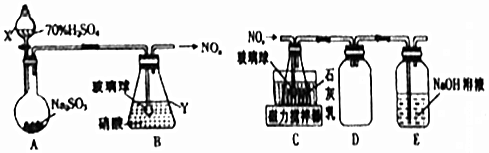
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
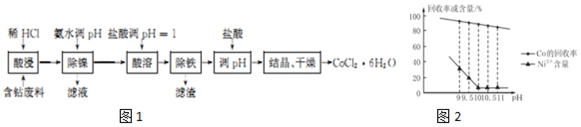
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.5 | 4.1 |
| Fe2+ | 7.5 | 9.7 |
| Co2+ | 6.6 | 9.4 |
| Ni2+ | 6.7 | 9.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| B. | 在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是Cu | |
| C. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| D. | 将Ba(OH)2溶液滴到明矾溶液中,当SO42-刚沉淀完时,铝以AlO2-的形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=12的溶液中.水电离出的c(OH-)定等于10-12mol/L | |
| B. | 将pH=2和pH=l2的酸碱溶液等体积混合后,溶液的pH一定等于7 | |
| C. | 若强酸、强碱中和后pH=7,则中和之前酸、碱的pH之和一定等于14 | |
| D. | 含等物质的量的HNO3、Na2CO3、CH3COOH的溶液混合后.溶液的pH一定大于7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com