
分析 (1)根据物质的量浓度c=$\frac{1000ρω}{M}$计算出镁离子的浓度,然后根据氯化镁的化学式组成计算出溶液中含有氯离子的物质的量浓度;
(2)用4.0mol•L-1的磷酸溶液和固体NaOH反应来配制2.0L混合液,H3PO4可与氢氧化钠反应生成NaH2PO4或Na2HPO4;每升混合液中含磷元素0.10mol,2.0L该混合液含有磷元素0.2mol,则反应后n(NaH2PO4)+n(Na2HPO4)=0.2mol,而NaH2PO4和Na2HPO4物质的量比为4:1,则n(NaH2PO4)=0.16mol,n(Na2HPO4)=0.04mol,根据磷、钠原子守恒,以此计算n(H3PO4)进而计算磷酸溶液的体积、n(NaOH)的物质的量,进而计算质量;
(3)根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,应结束后测得生成的气体体积比为甲:乙=1:2,由化学反应方程式2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,若铝粉足量,则铝粉和碱最多生成0.45mol氢气,铝粉和酸最多生成0.15mol氢气,而反应结束后测得生成的气体体积比为酸:碱=1:2,故碱生成的氢气不可能高于0.3mol,而氢氧化钠的量是一定的,那么只能是铝粉量对于碱来说不够,所以相对来说碱过量;而个时候的铝粉量对酸来说恰好足够,相对来说酸相比于铝粉来说就是不够的了;酸与金属反应时酸不足,碱与金属反应时碱过量,以此来计算解答.
解答 解:(1)氯化镁溶液的密度为d g•cm-3,其中镁离子的质量分数为A%,则该溶液中镁离子的浓度为:c(Mg2+)=$\frac{1000×d×A%}{24}$mol/L=$\frac{5dA}{12}$mol/L,
根据氯化镁的化学式可知该溶液中氯离子浓度为:c(Cl-)=2c(Mg2+)=$\frac{5dA}{12}$mol/L×2=$\frac{5dA}{6}$mol/L,
故答案为:$\frac{5dA}{6}$;
(2)用4.0mol•L-1的磷酸溶液和固体NaOH反应来配制2.0L混合液,H3PO4可与氢氧化钠反应生成NaH2PO4或Na2HPO4;则反应后n(NaH2PO4)+n(Na2HPO4)=0.2mol,而NaH2PO4和Na2HPO4物质的量比为3:1,则n(NaH2PO4)=0.2mol×$\frac{4}{4+1}$=0.16mol,n(Na2HPO4)=0.2mol×$\frac{1}{1+4}$=0.04mol,
由磷元素守恒可知需要n(H3PO4)=n(NaH2PO4)+n(Na2HPO4)=0.16mol+0.04mol=0.2mol,
磷酸溶液的体积V=$\frac{n}{c}$=$\frac{0.2mol}{4.0mol/L}$=0.05L=50mL,
由钠元素守恒可知需要n(NaOH)=n(NaH2PO4)+2n(Na2HPO4)=0.16mol+0.08mol=0.24mol,
则需要氢氧化钠的质量为:m(NaOH)=0.24mol×40g/mol=9.6g,
故答案为:50;9.6;
(3)解:盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×3mol/L=0.3mol,又两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,
则 2Al+6HCl═2AlCl3+3H2↑
6 3
0.3mol x
则:$\frac{6}{3}$=$\frac{0.3mol}{x}$,
解得:x=0.15mol,
一定条件下,气体的物质的量之比等于体积之比,
则碱与金属铝反应生成的氢气的物质的量为0.15mol×2=0.3mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,
则 2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
y 0.3mol
则:$\frac{2}{3}$=$\frac{y}{0.3mol}$,
解得:y=0.2mol,
则铝的质量为:0.2mol×27g/mol=5.4g,
故答案为:5.4.
点评 本题考查了物质的量浓度的计算、化学方程式的计算,题目难度中等,明确发生反应的实质为解答关键,试题知识点较多、综合性较强,充分考查了学生的分析能力及化学计算能力.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的NH4Cl溶液 | B. | 0.1 mol•L-1NaCl溶液 | ||
| C. | 0.1 mol•L-1氨水 | D. | 0.1 mol•L-1 NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和食盐水、浓硫酸 | B. | NaOH溶液、浓硫酸 | ||
| C. | NaHCO3溶液、硅胶 | D. | 浓盐酸、碱石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | HCl | C. | BaCl2 | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除②外 | B. | 除③外 | C. | 除②③⑤⑥外 | D. | 除③⑥外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列结论正确的是( )
,下列结论正确的是( )| A. | 该有机物分子式为C13H16,属于苯的同系物 | |
| B. | 1mol该有机物分子与溴水加成最多消耗5molBr2,与氢气加成最多消耗5molH2 | |
| C. | 该有机物分子至少有4个碳原子共直线,最多有13个碳原子共平面 | |
| D. | 一定条件下.该有机物可发生取代、加成和氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气不与石灰水反应 | |
| B. | Ca(OH)2能溶于水,澄清石灰水Ca(OH)2的含量少,吸收的尾气也很少 | |
| C. | 氯气与Ca(OH)2反应生成的CaCl2难溶于水 | |
| D. | 澄清石灰水能吸收空气中的CO2而边浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol NH5中含有5NA个N-H键(NA表示阿伏加德罗常数的值) | |
| B. | NH5中既有共价键又有离子键 | |
| C. | NH5的电子式为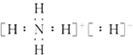 | |
| D. | 它与水反应的化学方程式为NH5+H2O═NH3•H2O+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com