
| A. | v(D)=0.01 mol/(L•s) | B. | v(C)=0.8 mol/(L•min) | ||
| C. | v(B)=0.02 mol/(L•s) | D. | v(A)=0.5 mol/(L•min) |
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同 | |
| B. | 若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4 | |
| C. | 若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m | |
| D. | Mm+离子一定不能与酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  量取20.00 mL Na2CO3溶液 | B. |  能证明非金属性 Cl>C>Si | ||
| C. | 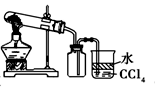 实验室制取并收集NH3 | D. | 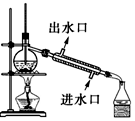 分离酒精与CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离的c(H+):①=②>③=④ | |
| B. | 将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②=③ | |
| C. | 等体积的①、②两种溶液分别与足量铝粉反应,生成H2的量相等 | |
| D. | 向等体积四种溶液中分别加水至体积为原来的100倍后,溶液的pH:③>④>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
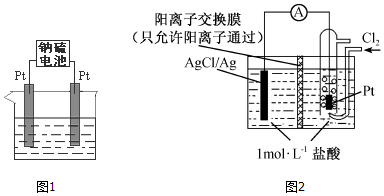
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | W、Y、X三种元素的原子半径依次减小 | |
| B. | Z元素的气态氢化物的热稳定性比Y的高 | |
| C. | W元素与氢元素可能会形成W2H6 | |
| D. | Y元素的单质能从NaZ溶液中置换出Z元素的单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com