
【题目】Al及其化合物在现代工业中有广泛的用途。回答下列问题:
(1)下列状态的铝中,电离最外层的一个电子所需能量最小的是_____(填标号)。
A [Ne]3s1 B [Ne]3s2 C [Ne]3s23p1 D [Ne] 3s13p2
(2)熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为_____(标出配位键);其中Al的配位数为_________。二聚体A12C16中Al原子的轨道杂化类型是________。
(3) 实际上,偏铝酸钠在水溶液中都是以Na[Al(OH)4]和形式存在,1mol Na[Al(OH)4]中含有σ键的数目为_________。
(4)Ga(镓)和铝是同一主族元素,Ga原子的电子排布式是___________。
【答案】D 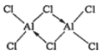 4 sp3 8NA [Ar]3d104s24p1
4 sp3 8NA [Ar]3d104s24p1
【解析】
(1)电离最外层的一个电子所需能量:基态>激发态,第一电离能<第二电离能<第三电离能,据此判断解答;
(2) 二聚体Al2Cl6中Al原子有空轨道,Cl可以提供孤电子对形成配位键;配合物中的配位数是指直接同中心离子(或原子)配位的原子数目;双分子Al2Cl6中Al原子形成4个σ键,没有孤对电子,杂化轨道数目为4;
(3) Na[Al(OH)4]是离子化合物,[Al(OH)4]-中,铝离子含有空轨道,水分子含有孤对电子对,铝离子与水分子之间形成配位键,铝离子配体数为4,1个OH-含1个O-H键,则[Al(OH)4]-含有8个σ键;
(4)Ga元素原子核外电子数为31,根据能量最低原理书写核外电子排布式。
(1)A.[Ne]3s1再失去一个电子为Al的第三电离能;
B.[Ne]3s2再失去一个电子为Al的第二电离能;
C.[Ne]3s23p1为基态铝原子核外电子排布式,失去一个电子为Al的第一电离能;
D.[Ne] 3s13p2为激发态铝原子核外电子排布式;
铝的第三电离能>第二电离能>第一电离能,基态大于激发态,所以电离最外层一个电子所需能量最小的为D,答案选D;
(2)熔融时AlCl3生成可挥发的二聚体Al2Cl6,该二聚体由Al提供空轨道,Cl原子提供电子对形成配位键,其结构式为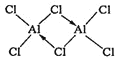 ;配合物中的配位数是指直接同中心离子(或原子)配位的原子数目,二聚体Al2Cl6中与Al直接相连的原子有4个,故其配位数为4;由双分子Al2Cl6的结构可知,分子中Al原子形成4个σ键,没有孤对电子,杂化轨道数目为4,Al原子采取sp3杂化;
;配合物中的配位数是指直接同中心离子(或原子)配位的原子数目,二聚体Al2Cl6中与Al直接相连的原子有4个,故其配位数为4;由双分子Al2Cl6的结构可知,分子中Al原子形成4个σ键,没有孤对电子,杂化轨道数目为4,Al原子采取sp3杂化;
(3)Na[Al(OH)4]是离子化合物,[Al(OH)4]-中,铝离子含有空轨道,水分子含有孤对电子对,铝离子与水分子之间形成配位键,铝离子配体数为4,1个OH-含1个O-H键,则[Al(OH)4]-含有8个σ键,1mol Na[Al(OH)4]中含有σ键的数目为8NA;
(4)Ga元素原子核外电子数为31,Ga基态原子的核外电子排布式是:1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)。


科目:高中化学 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2 ②KClO3+6HCl=3Cl2+KCl+3H2O ③ 2KBrO3+Cl2=Br2+2KClO3,下面说法正确的
A.上述三个反应都有单质生成,所以都是置换反应
B.反应②中还原剂与氧化剂的物质的量之比为6:1
C.反应③中1mol Cl2反应,则氧化剂得电子的物质的量为10mol
D.氧化性由强到弱的顺序为:KClO3>KBrO3>Cl2>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】著名的“侯氏制碱法”主要反应原理是:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。若实验室根据此原理制备少量的Na2CO3,主要实验包括:制取NH3和CO2→生成NaHCO3→分离NaHCO3→制取Na2CO3 四个步骤。下列实验选用的主要仪器或主要步骤不正确的是

A. 制取氨气,可选用②③
B. 分离 NaHCO3,可选用④⑤⑦
C. 制取 Na2CO3,可选用①②⑦⑧
D. 制取 NaHCO3时,应先在⑨中通入CO2后再加入氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】mA(g)+nB(g) ![]() pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是:( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是:( )
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变 ④各组分的质量分数不再改变⑤反应速率VA:VB:VC:VD=m:n:p:q ⑥单位时间内m mol A断键反应,同时p mol C也断键反应
A. ③④⑤⑥ B. ②③④⑥ C. ①③④⑤ D. ①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 均为短周期主族元素,
均为短周期主族元素,![]() 、
、![]() 处于同一周期,
处于同一周期,![]() 、
、![]() 的最低价离子分别为
的最低价离子分别为![]() 和
和![]() ,
,![]() 和
和![]() 具有相同的电子层结构。下列说法正确的是( )
具有相同的电子层结构。下列说法正确的是( )
A.原子的最外层电子数:![]()
B.阴离子还原性:![]()
C.离子半径:![]()
D.原子序数:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表中短周期的一部分,若A元素原子的最外层电子数比次外层电子数少3,则下列说法正确的是( )
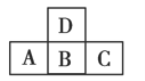
A.四种元素都是非金属元素
B.B与D之间能形成三种常见的化合物
C.A与C的原子序数之和跟B与D的原子序数之和相等
D.四种元素形成的单质在常温下都是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解AgNO3溶液,说法不正确的是( )
A.电解过程中阴极质量不断增加
B.电解过程中溶液的pH不断降低
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是CsCl晶体的晶胞(晶体中最小的重复单元)已知晶体中2个最近的Cs+核间距离为acm,氯化铯的式量为M,NA为阿伏加德罗常数,则CsCl晶体的密度为(单位:g/cm)
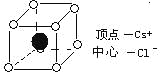 ( )
( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com