


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
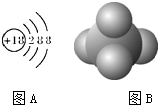
| A、Cl-离子的结构示意图:如图A |
| B、H2O2的结构式:H-O-O-H |
| C、乙烯的结构简式:CH2CH2 |
| D、CCl4分子的球棍模型:如图B |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量位居第一位 |
| Z | 短周期中,其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
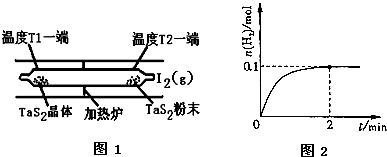
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 无机化合物可根据其组成和性质进行分类.
无机化合物可根据其组成和性质进行分类.| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ② |
③ ④Ba(OH0)2 |
⑤Na2CO3 ⑥ |
⑦CO2 ⑧Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最高正价为+7价的一种元素 |
| B、除最外层电子外,其余各层都达到饱和的一种元素 |
| C、原子L层比M层多6个电子的一种元素 |
| D、最外层电子数为8的一种元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com