
【题目】胶体最本质的特征是( )
A.丁达尔效应
B.可以通过滤纸
C.布朗运动
D.分散质粒子的直径在10﹣9~10﹣7 m之间
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)
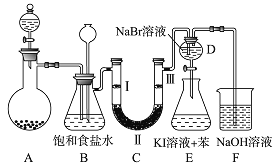
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的离子反应方程式为:_____________.装置 B 中饱和食盐水的作用是_________________;
若C处发生了堵塞,则B中的现象为__________________.
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ应该依次放入____(填编号)
① | ② | ③ | ④ | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为______色,说明________________;打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是__________________;
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为_____.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用的漂白液,同时有 NaHCO3 生成,该反应的化学方程式是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,所用仪器合理的是( )
A. 在坩埚中放入NaCl溶液,加热、蒸发得到NaCl晶体
B. 用10 mL的量筒量取4.8 mL的盐酸
C. 用托盘天平称取25.20 g NaCl
D. 用1000 mL容量瓶配制450 mL 0.1 mol·L-1的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室进行下列实验,括号内的实验用品都能用到的是
A. 钠的焰色反应(铂丝、氯化钠溶液、稀盐酸)
B. 蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液)
C. 硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体)
D. 肥皂的制取(蒸发皿、玻璃棒、甘油)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热条件下浓硫酸能将木炭粉氧化成CO2,本身被还原成SO2。试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
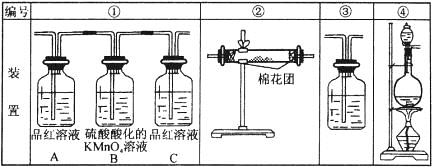
(1)这些装置的连接顺序是(按产物气流从左至右的方向,填写装置的编号):______→____→____→____。
(2)实验时可观察到装置①中A瓶的溶液褪色。A瓶溶液的作用是_________,B瓶溶液的作用是_______, C瓶溶液的作用是________________。写出B中发生的离子方程式__________。
(3)装置②中所加的固体药品是____________,可验证的产物是____________。
(4)装置③中所盛溶液是_____________,可验证的产物是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应式为:Li+2Li0.35NiO2![]() 2Li0.85NiO2,下列说法不正确的是( )
2Li0.85NiO2,下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-===Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质溶液
D.放电过程中Li+向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙酸的分子式:C2H4O B. 乙烯的结构简式: CH2CH2
C. 乙酸的结构简式:CH3CH2OH D. 乙酸乙酯的结构简式:CH3 COO CH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中,进行化学反应:2X(g) + Y(s)![]() Z(g) + W(g);若其化学平衡常数(K)和温度(t)的关系如下表:
Z(g) + W(g);若其化学平衡常数(K)和温度(t)的关系如下表:
t/℃ | 700 | 800 | 900 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.3 | 1.8 | 2.7 |
对该反应而言,下列说法正确的是 ( )
A. 该反应正反应为放热反应
B. 起始浓度不变,K越大,反应物的转化率越大
C. 温度不变,增加X的用量,K增大
D. 达平衡后,加入催化剂,K增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com