
下列元素中,最高正化合价数值最大的是
A.C B.S C.F D.Ne
 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
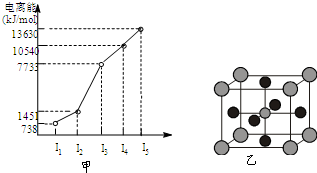 有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.
有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第三周期元素原子半径 Cl<S<Na | B、在卤化氢中HF最不稳定 | C、在钠、钾、铷三种单质中,钠的熔点最高 | D、主族元素的最高正化合价一般等于其最外层电子数 |
查看答案和解析>>
科目:高中化学 来源:2014届山西省等四校高三第一次联考化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中;常温下,Z的单质能溶于W的最高价氧化物对应水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是
A.通过电解熔融的Z、Q形成的化合物可制取Z单质
B.原子半径的大小顺序为W>Q>Z>X>Y
C.元素Y的最高正化合价为+6
D.XQ3分子中,中心原子是sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中;常温下,Z的单质能溶于W的最高价氧化物对应水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是
A. 通过电解熔融的Z、Q形成的化合物可制取Z单质
B. 原子半径的大小顺序为W>Q>Z>X>Y
C. 元素Y的最高正化合价为+6
D. XQ3分子中,中心原子是sp3杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com