
 已知乙烯能发生以下转化:
已知乙烯能发生以下转化:| 一定条件下 |
| 一定条件下 |
| Cu |
| △ |
| Cu |
| △ |
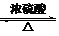 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,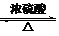 CH3COOCH2CH3+H2O;酯化反应(或取代反应).
CH3COOCH2CH3+H2O;酯化反应(或取代反应).


科目:高中化学 来源: 题型:
| A、该反应中的氧化剂是Cl2 |
| B、SO2与氯水的漂白原理相同,所以可用S02做纺织工业的漂白剂 |
| C、上述反应中,每生成1mol SO42-,可脱去2mol Cl2 |
| D、根据该反应可判断还原性:S2O32->Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 将除去氧化镁的Mg条投入到盛有10mL0.1mol?L-1HCl溶液的试管中,发现H2发生的速率变化如右图所示,其中时间t1~t2段速率变化的主要原因是
将除去氧化镁的Mg条投入到盛有10mL0.1mol?L-1HCl溶液的试管中,发现H2发生的速率变化如右图所示,其中时间t1~t2段速率变化的主要原因是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验操作 | 现象 | 解释(用离子方程式表示) |
| 向其中一份加入少量氯水 | ||
| 向另一份加入少量氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷和乙烯:分别通入酸性KMnO4溶液 |
| B、乙醇和乙酸:分别滴加NaOH溶液 |
| C、苯和四氯化碳:分别与水混合、振荡、静置 |
| D、棉花织品和羊毛织品:分别燃烧闻气味 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com