
 2NaHSO4+MnSO4+2H2O+I2
2NaHSO4+MnSO4+2H2O+I2 2Na2SO4+3NaHSO4+H2O+I2
2Na2SO4+3NaHSO4+H2O+I2

科目:高中化学 来源:不详 题型:单选题
| A.实验室用NH4Cl 和Ca(OH)2制备NH3 |
| B.工业上电解熔融状态Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 |
| D.Na2O2用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应中还原剂是S2O32﹣ |
| B.H2O参与该反应,且作氧化剂 |
| C.根据该反应可判断氧化性:Cl2>SO42﹣ |
| D.上述反应中,每生成l mol SO42﹣,可脱去2mol Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
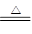 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应显示硫酸具有酸性 | B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 | D.反应中硫酸作氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述反应属于氧化还原反应 |
| B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) |
| C.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替 |
| D.上述反应中消耗3molP时,转移电子的物质的量为15mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 下列说法正确的是
下列说法正确的是| A.Cr2O72-被氧化成CrO5 | B.该反应为氧化还原反应 |
| C.反应中H2O2被还原成H2O | D.此反应用于检验Cr2O72-离子的存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com