
��֪����1molH2�����л�ѧ������ʱ��Ҫ����436kJ������
��1molCl2�����л�ѧ������ʱ��Ҫ����243kJ������
����Hԭ�Ӻ�Clԭ���γ�1molHCl����ʱ�ͷ�431kJ������
����������ȷ����
A��������������Ӧ�����Ȼ���������Ȼ�ѧ����ʽ��H2��g��+Cl��g����2HCl��g��
B��������������Ӧ����2mol�Ȼ������壬��Ӧ�ġ�H��183kJ/mol
C��������������Ӧ����2mol�Ȼ������壬��Ӧ�ġ�H����183kJ/mol
D��������������Ӧ����1mol�Ȼ������壬��Ӧ�ġ�H����183kJ/mol

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣�����ȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��2H2(g)��O2(g)===2H2O(l)����H����572 kJ��mol��1����ش��������⣺
(1)�����������ܺ�________(����ڡ�����С�ڡ����ڡ�)��Ӧ�������ܺ͡�
(2)��2 mol������ȫȼ������ˮ��������ų�������________(����ڡ�����С�ڡ����ڡ�)572 kJ��
��3����Ӧ2H2+ O2 �� 2H2O �������仯��ͼ��ʾ����֪��1molH2��1molO2��1molH-O�еĻ�ѧ���ֱ���Ҫ����436KJ��496KJ��463KJ��������Ӧ���̣��� ������ա��ų����� KJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��֪��1molH2��Ҫ����436kJ��������1molO2��Ҫ����496kJ�������γ�ˮ�����е�1molH��O�ܹ��ͷ�463kJ�����������������������ݼ��㷴Ӧ��
2H2(g)+O2(g)=2H2O(g) ����H = ��
��2����ͼ��ʾ�����γ�����ȼ�ϵ�ء�ͨ������ȼ�ϵ������ʽ(���������ҺΪH2SO4��Һʱ)�ͼ�ʽ[���������ҺΪNaOH(aq)��KOH(aq)ʱ]���֡��Իش��������⣺
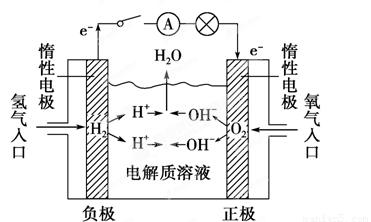
����ʽ��صĵ缫��Ӧ������________________������______________������ܷ�Ӧ��______________���������ҺpH�ı仯________(��������С�����䡱)��
�ڼ�ʽ��صĵ缫��Ӧ������________________������______________������ܷ�Ӧ��______________���������ҺpH�ı仯________(��������С�����䡱)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com