
| 1×10-13 |
| 1×10-12 |
| 0.1Va-0.01Vb |
| Va+Vb |
| 1×10-13 |
| 1×10-10 |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
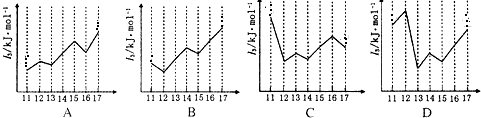
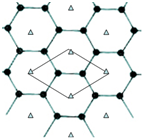
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3通入FeSO4溶液中 |
| B、CO2通入CaCl2溶液中 |
| C、AlCl3溶液中滴入NaHCO3溶液 |
| D、SO2通入Ba(NO3)2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取35.20g NaCl |
| B、用10ml量筒量取8.5ml盐酸 |
| C、用50ml烧杯量取15.80ml溶液 |
| D、用250ml容量瓶量取25ml溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2O |
| B、NO |
| C、N2O3 |
| D、NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡一定向正反应方向发生了移动 |
| B、平衡一定向逆反应方向发生了移动 |
| C、反应物浓度相应减小 |
| D、平衡可能发生了移动,也可能没有发生移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com