
| A. | Na2Mn5O10是氧化产物 | |
| B. | 正极反应式:Ag-e-═Ag+ | |
| C. | Cl-不断向“水”电池的正极移动 | |
| D. | 毎转移2mol电子,负极质量增加71克 |
分析 根据电池总反应可判断出反应中Ag的化合价升高,被氧化,Ag应为原电池的负极,AgCl是氧化产物;方程式中MnO2生成Na2Mn5O10,Mn化合价降低,所以MnO2为氧化剂,生成Na2Mn5O10为还原产物;在原电池中阴离子向负极移动,阳离子向正极移动,以形成闭合电路.
解答 解:A、反应中Mn化合价降低,被还原,所以MnO2为氧化剂,生成Na2Mn5O10为还原产物,故A错误;
B、根据电池总反应:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,可判断出Mn化合价降低,MnO2应为原电池的正极,发生反应的电极方程式为:5MnO2+2e-=Mn5O102-,故B错误;
C、在原电池中阴离子向负极移动,阳离子向正极移动,所以Cl-不断向“水”电池的负极移动,故C错误;
D、Ag应为原电池的负极,负极发生反应的电极方程式为:Ag+Cl--e-=AgCl,所以毎转移2mol电子,负极质量增加2×35.5=71克,故D正确;
故选:D.
点评 本题考查原电池的电极反应和离子的定向移动以及电化学的简单计算,做题时要注意总电池反应式的判断利用,运用两极上的反应特点做题,分析Mn元素的化合价变化是该题的难点.


科目:高中化学 来源: 题型:选择题
| A. | pH:②>③>④>① | B. | c(CH3COO-):②>④>③>① | ||
| C. | c(H+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
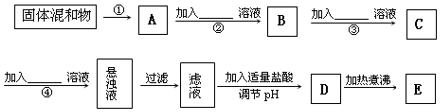
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应 | |
| B. | Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO3固体,铜粉会溶解 | |
| D. | 金属单质Na、Mg、Fe在一定条件下与水反应都生成H2和相应的碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②④ | C. | ①②⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用活性炭除去冰箱中的异味 | B. | 用米汤检验含碘食盐中的KIO3 | ||
| C. | 用食醋除去热水壶中的水垢 | D. | 用NaOH溶液鉴别地沟油和矿物油 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
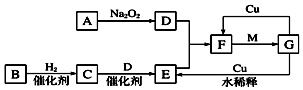
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY | B. | XY2 | C. | XY3 | D. | XY4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com