
| A. | ①②⑤ | B. | ①④⑤ | C. | ②④⑤ | D. | ①③⑤ |
科目:高中化学 来源: 题型:选择题
| A. | 在强碱性溶液中能大量存在:Na+、K+、Cl-、NH4+ | |
| B. | 加入金属铝后溶液中有大量气泡产生的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| C. | 含有大量Fe3+的溶液中:SCN-、I-、K+、Br- | |
| D. | 溶液通入足量氨气后各离子还能大量存在:K+ Na+ OH-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

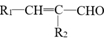 +H2O
+H2O +R2-OH$\stackrel{一定条件}{→}$
+R2-OH$\stackrel{一定条件}{→}$ +HCl
+HCl .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于稀盐酸中:CO32-+2H+═H2O+CO2↑ | |
| B. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| C. | 铁与稀盐酸反应:2Fe+6H+═3H2↑+2Fe3+ | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑧ | B. | ③⑥⑨⑩ | C. | ④⑤⑥⑧ | D. | ④⑤⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2是还原产物 | |
| B. | 有 0.250 mol KNO3 被氧化 | |
| C. | NaN3中氮元素为-3 价 | |
| D. | 被氧化的 N 原子的物质的量为 3.75mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 用途 | 解释 |
| A | 可用FeCl3溶液刻蚀铜制电路板 | Fe3+的氧化性强于Cu2+ |
| B | 碳与石英反应可冶炼粗硅 | 碳的非金属性比硅强 |
| C | 四氯化碳可用于灭火 | 四氯化碳的沸点高 |
| D | 酸性KMnO4溶 液可漂白织物 | KMnO4有强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com