
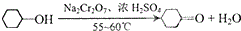 实验室用Na2Cr2O7氧化环己醇制取环己酮(已知该反应为放热反应):
实验室用Na2Cr2O7氧化环己醇制取环己酮(已知该反应为放热反应):| 物质 | 沸点( ) | 密度(g.cm-3,20) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.9624 | 能溶于水和乙醚 |
| 环己酮 | 155.6(95) | 0.9478 | 微溶于水,能溶于乙醚 |
| 水 | 100.0 | 0.9982 |
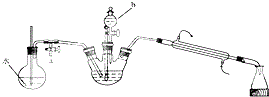
分析 (1)由仪器结构特征,可知仪器b为分液漏斗;根据浓硫酸稀释操作进行解答;
(2)反应为放热反应,一次性加入会放出大量的热,温度过高会导致副反应发生;
(3)利用水蒸气与环己酮形成的具有固定组成的混合物,进行蒸馏出产品环己酮;圆底烧瓶中玻璃管内的水位上升过高时,说明装置内压强过大,应立即打开活塞a降低装置内压强;
(4)有机层的密度小于水,有机层在上层;乙醚以挥发,利用水浴加热进行蒸馏除去乙醚;
(5)根据环己醇的质量计算环己酮的理论产量,产率=(实际产量÷理论产量)×100%.
解答 解:(1)由仪器结构特征,可知仪器b为分液漏斗;重铬酸钠溶液与浓硫酸混合操作为:将浓硫酸缓慢加入重铬酸钾溶液中,并不断搅拌,
故答案为:分液漏斗;将浓硫酸缓慢加入重铬酸钾溶液中,并不断搅拌;
(2)反应为放热反应,一次性加入会放出大量的热,故应分多次加入,防止温度过高发生副反应,
故答案为:防止温度过高发生副反应;
(3)步骤③实验操作的目的是:水蒸气与环己酮形成的具有固定组成的混合物,蒸馏出产品环己酮;圆底烧瓶中玻璃管内的水位上升过高时,说明装置内压强过大,应立即打开活塞a降低装置内压强,防止爆炸危险发生,
故答案为:水蒸气与环己酮形成的具有固定组成的混合物,蒸馏出产品环己酮;打开活塞a;
(4)有机层的密度小于水,有机层在上层;乙醚以挥发,利用水浴加热进行蒸馏除去乙醚,
故答案为:上;水浴加热;
(5)环己酮的理论产量为20g×$\frac{98}{100}$=19.6g,故产率=(12g÷19.6g)×100%=61.2%,
故答案为:61.2.
点评 本题考查有机实验制备,涉及仪器识别、浓硫酸稀释、对装置与操作的分析评价、物质的分离提纯、产率计算等,难度中等,是对学生综合能力的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 都能溶于水,但溶解性都比乙醇的差 | |
| B. | 都能与金属钠反应放出氢气 | |
| C. | 苯酚是比碳酸更强的酸,环己醇则显中性 | |
| D. | 苯酚与FeCl3溶液作用显紫色,环乙醇加入FeCl3溶液中无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 物质A、E、F的焰色反应呈黄色,物质I的1个分子由4个原子组成并共含有10个电子,B、C、D、K在常温下都是气体单质,G在常温下是无色液体,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如图所示(部分反应条件已略去):
物质A、E、F的焰色反应呈黄色,物质I的1个分子由4个原子组成并共含有10个电子,B、C、D、K在常温下都是气体单质,G在常温下是无色液体,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如图所示(部分反应条件已略去):
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 21.6g | B. | 26.8g | C. | 23.4g | D. | 31.9g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知某种气态化石燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收).
已知某种气态化石燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收).| 实验前 | 实验后 | |
| (干燥剂+U形管)的质量 | 101.1g | 102.9g |
| (石灰水+广口瓶)的质量 | 312.0g | 314.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯乙烯使溴水褪色;加成反应 | |
| B. | 乙烯水化生成乙醇;取代反应 | |
| C. | 乙醇与CuO加热反应生成乙醛;氧化反应 | |
| D. | 无水乙醇与浓硫酸加热到170℃制取乙烯;消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热时无气体放出 | |
| B. | 溶于水后滴加稀BaCl2溶液有白色沉淀生成 | |
| C. | 滴加盐酸时有气泡放出 | |
| D. | 溶于水后滴加澄清石灰水有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com