
分析 依据方程式,结合平衡等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积进行计算;
解答 解:17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol•L-1、c(N2O4)=0.0120mol•L-1.则反应2NO2(g)?N2O4(g)的平衡常数K=$\frac{c(N{\;}_{2}O{\;}_{4})}{{c}^{2}(NO{\;}_{2})}$=$\frac{0.0120}{0.0300{\;}^{2}}$=13.3L/mol;
答:平衡常数为13.3.
点评 本题考查化学平衡常数计算,难度不大,答题时注意根据平衡常数的定义进行计算.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:填空题
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | m mol SO2、n mol O2、p mol SO3 |
| c(SO3)/mol•L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
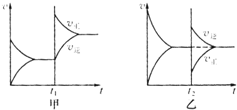 在一定条件下,有反应xA+yB?zC.
在一定条件下,有反应xA+yB?zC.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 10 | 20 | 30 | 40 | 50 | 60 |
| n(CH3OH)/mol | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②③ | C. | 只有②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体一定含CO32- | |
| B. | 某无色溶液滴入酚酞试液显红色,该溶液呈碱性 | |
| C. | 某溶液中滴加BaCl2溶液生成不溶于稀硝酸的白色沉淀,该溶液可能含有SO42- | |
| D. | 验证烧碱溶液中是否含Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com