
 ���ķ�ˮ�������������س�ȥ����ԭ����ͼ1��ʾ��
���ķ�ˮ�������������س�ȥ����ԭ����ͼ1��ʾ��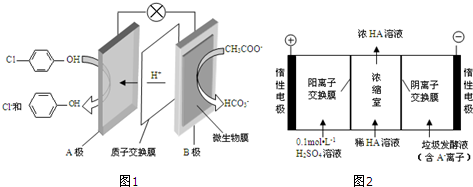
| ||
| ||
 -OH+2e-+H+�T
-OH+2e-+H+�T -OH+Cl-���ʴ�Ϊ��Cl-
-OH+Cl-���ʴ�Ϊ��Cl- -OH+2e-+H+�T
-OH+2e-+H+�T -OH+Cl-��
-OH+Cl-��| 1 |
| 2 |
| 145g?L-1-10g?L-1 |
| 90g/mol |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Һ��ͨ��CO2����������ɫ������ͨ�����˿ɷ�������� |
| B���ζ�ʵ��ʱ����ƿ������ˮϴ����ֱ��ʢ����Һ |
| C�����������������ϡ���ᷴӦ����S��SO2���ڶ����ⶨ��Ӧ����ʱ���ȿ���S�Ա���ڸǷ���Ҳ������ˮ����SO2������������ķ�Ӧ���� |
| D��ij��Һ���������ữ��BaCl2��Һ�����а�ɫ�������ɣ���ԭ��Һ����SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�м���������CH3COONa |
| B����ˮ�м���������NaHSO4 |
| C����ˮ�м���NaI��������100�棬pH=6 |
| D����ˮ�м�������KAl��SO4��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| pH | 4.13 | 5.50 | 7.00 | 8.00 | 9.00 | 10.10 | 11.20 | 13.20 |
| V��O2��/mL | 9.0 | 90 | 467 | 595 | 639 | 550 | 500 | 455 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
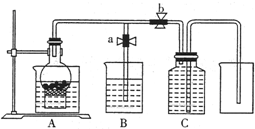 ijͬѧ�����ͼ��ʾװ���������ô�������ijŨ��ϡ���ᷴӦ��ȡNO���壮
ijͬѧ�����ͼ��ʾװ���������ô�������ijŨ��ϡ���ᷴӦ��ȡNO���壮
|
������Һ�е������Ӽ������ʵ��� | ||||
��
|
|||||
=
|
a mol Fe3+ | ||||
����
|
|||||
=
|
a mol Fe2+ | ||||
��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
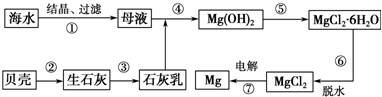
| A���ô˷���ȡþ���ŵ�֮һ��ԭ����Դ�ḻ |
| B������ߵ��MgCl2ʱ������������ |
| C������ɽ���������HCl��������ˮ |
| D�����������������漰���ϡ��ֽ���ֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
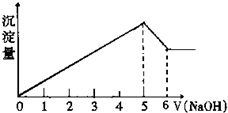 ��һþ�����Ͻ�������ϡ������ǡ����ȫ�ܽ⣬�ټ�������������Һ���������������ʵ���������������Һ������仯��ͼ��ʾ����Ͻ���þ���������ʵ���֮��Ϊ��������
��һþ�����Ͻ�������ϡ������ǡ����ȫ�ܽ⣬�ټ�������������Һ���������������ʵ���������������Һ������仯��ͼ��ʾ����Ͻ���þ���������ʵ���֮��Ϊ��������| A��2��1 | B��4��1 |
| C��1��1 | D��1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
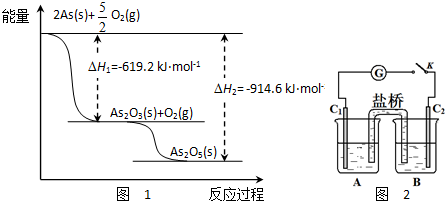
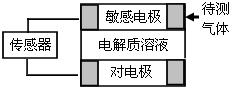 ������Զ�������г���Ӧ��ԭ���ԭ������ͼΪ�õ�ع�����ʾ��ͼ��������ɢ�������е缫��������Ӧ���������ͻ���յ����źţ��±��г��˴������弰���е缫�ϲ��ַ�Ӧ������Ե缫���������е缫��Ӧ�෴�ĵ缫��������˵������ȷ���ǣ�������
������Զ�������г���Ӧ��ԭ���ԭ������ͼΪ�õ�ع�����ʾ��ͼ��������ɢ�������е缫��������Ӧ���������ͻ���յ����źţ��±��г��˴������弰���е缫�ϲ��ַ�Ӧ������Ե缫���������е缫��Ӧ�෴�ĵ缫��������˵������ȷ���ǣ�������| �������� | ���ֵ缫��Ӧ���� |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
| A�����Cl2ʱ���������Һ�е������������е缫�ƶ� |
| B���ϱ�������ʱ�����е缫����������� |
| C����⺬��ͬ���ʵ�����H2S��CO���ݿ�������ʱ���������������ĵ������ʵ���֮��Ϊ4��1 |
| D�����H2S����ʱ���ڶԵ缫�ϳ���������Ե缫�ϵĵ缫��ӦʽΪ��O2+2H2O+4e-�T4OH- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com