
| ||
| ||
| ||
| ||


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
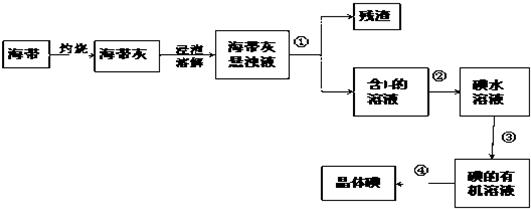
查看答案和解析>>
科目:高中化学 来源: 题型:
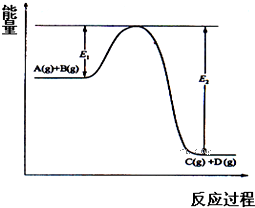 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
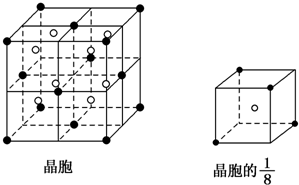 A、B、C、D、E都是元素周期表中的前20号元素,原子序数依次增大,B、C、D同周期,A、D原子中某p能级均排有5个电子,E和其他元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水.
A、B、C、D、E都是元素周期表中的前20号元素,原子序数依次增大,B、C、D同周期,A、D原子中某p能级均排有5个电子,E和其他元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水.| 1 |
| 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
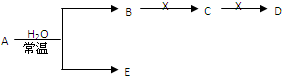
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在恒容的密闭容器中混合气体的密度不变 |
| B、在恒容的密闭容器中混合气体的压强不变 |
| C、A、B、C的浓度之比为1:2:1,且保持不变 |
| D、A的消耗速率与C的生成速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将含有SO2的CO2气体通过足量的饱和Na2CO3溶液以除去SO2 |
| B、称取19.0g氯化亚锡(SnCl2),用100mL蒸馏水溶解,配制1.0mol/L SnCl2溶液 |
| C、用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱 |
| D、测定NaCl和NaF溶液的pH值,确定F、Cl两元素非金属性的强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com