
| ||
| ||


科目:高中化学 来源: 题型:
| A、150ml 1mol?L-1NaCl溶液 |
| B、75ml 2mol?L-1 KClO3溶液 |
| C、150ml 2mol?L-1 KCl溶液 |
| D、75ml 1mol?L-1 FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下任何气体的分子间距离几乎相等 |
| B、固体和液体粒子之间的距离和忽略不计 |
| C、构成气体的粒子的大小相对于它们之间的距离可忽略不计 |
| D、一定温度和压强下各种气态物质所占体积的大小,由构成气体的分子大小决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
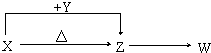 X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):
X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):查看答案和解析>>
科目:高中化学 来源: 题型:
A、熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH
| ||||
| B、AlCl3溶液中通入过量的NH3:Al3++4NH3?H2O=AlO2-+4NH4+ | ||||
C、红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O(g)
| ||||
| D、“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
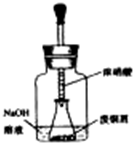 实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:
实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com