
【题目】实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2 CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
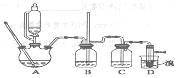
有关数据列表如下:
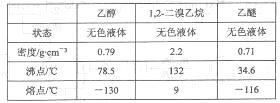
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是
______________;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入____,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是______________________;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____层(填“上”或“下”);
(5)连接有长玻璃导管的装置B的作用是__________________;
(6)若产物中有少量副产物乙醚,可用__________________的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是__________________;但又不能过度冷却(如用冰水),其原因是__________________。
【答案】 d c 溴的颜色完全褪去 下 安全瓶 蒸馏 乙烯与溴反应时放热,冷却可避免溴的大量挥发 1,2二溴乙烷的凝固点较低(9 ℃),过度冷却会使其凝固而使气路堵塞
【解析】(1)乙醇在浓硫酸140℃的条件下,发生分子内脱水,生成乙醚,故答案为:d;
(2)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,故答案为:c;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,故答案为:溴的颜色完全褪去;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,故答案为:下;
(5)连接有长玻璃导管的装置B与外界大气连通,能起到安全瓶的作用,防止倒吸。
(6)1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离,故答案为:蒸馏;
(7)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,故答案为:乙烯与溴反应时放热,冷却可避免溴的大量挥发;1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞


科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是( )
A. Na+ H+ NO3- Fe2+ B. Ca2+ H+ ClO- NO3-
C. K+ H+ Cl- SO42- D. Fe3+ Cl- H+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)除去自来水中的Ca2+、Mg2+、Cl—、SO42—等杂质,选择装置_____________(填代表装置图的字母)。
(2)用CCl4萃取碘水中的I2,有机层的颜色为___________________。
(3)装置A中①的名称是_____________,进水的方向是_____________。装置B在分液时为使液体顺利滴下,应进行的具体操作是_____________。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。
正确的操作顺序是_____________(填写字母)。
a.⑤②③①⑥④⑦b.⑤①②③⑥④⑦ c.⑤③②①⑥④⑦d.⑤②①③④⑥⑦
问题2:由海水到氯化钠晶体的实验过程中要用到的主要装置是_____________(从给定的四种装置中选择,填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列盐溶液的酸碱性,能发生水解的用离子方程式表示,不能发生水解的请写上“不发生水解”字样。
K2CO3溶液呈 性 ;
K2SO4溶液呈 性 ;
FeCl3溶液呈 性 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列变化:①Na2CO3→Na2SiO3,②SiO2→H2SiO3,③Na2SiO3→Na2CO3,④CaO→CaSiO3,其中不能通过一步反应实现的是
A. 只有① B. ②④ C. 只有② D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中将2molNaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(n)的取值范围是( )
A. n≥1 B. 1<n<2 C. 2≤n<4 D. n≥4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3COOH分别跟H﹣18O﹣C2H5和H﹣16O﹣C2H5酯化反应后,两者生成的水分子的相对分子质量( )
A.前者大B.前者小C.相等D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-.
Ⅰ.某校研究性学习小组设计如图流程以回收铜和硫酸亚铁.请回答:

(1)反应①的离子方程式为__________________。
(2)操作①中用到的玻璃仪器是_______________(填序号)。
a.烧杯 b.漏斗 c.玻璃棒 d.酒精灯
(3)固体成份是_________________(填名称)。
(4)原料②的名称为__________________。
Ⅱ.已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3—、MnO4—、IO4—离子,有关离子反应方程式为:_______________________,用双线桥标出上述反应的电子得失____________________________________。在锰离子转化为高锰酸根离子的反应中,如果把反应后的溶液稀释到1升,测得溶液的pH=2,则在反应中转移电子的物质的量为_______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com