
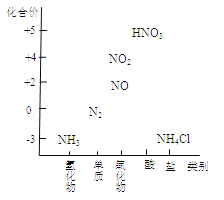
【题目】下图为氮及其化合物的类别与化合价对应的关系图。
(1)实验室制取氨气。
① 化学方程式是_______。
② 可用向下排空气法收集氨气的原因是_______。
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是_______。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2 ![]() 2NO。
2NO。
b. 氨的催化氧化:_________。
② 体现N元素的氧化性:_________。
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。
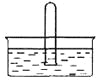
① NO2溶于水的化学方程式是_________。
② 使试管中NO2完全被水吸收的操作是________。
【答案】2NH4Cl+Ca(OH)2![]() CaCl2 +2NH3↑+2H2O 氨气的密度小于空气的密度 氨气易溶于水,使装置中的压强小于外界的压强,引起倒吸 4NH3 + 5O2
CaCl2 +2NH3↑+2H2O 氨气的密度小于空气的密度 氨气易溶于水,使装置中的压强小于外界的压强,引起倒吸 4NH3 + 5O2![]() 4NO + 6H2O 3Cu+8HNO3=3Cu(NO3)2 +2NO↑+4H2O 3NO2+H2O=2HNO3+NO 缓缓通入
4NO + 6H2O 3Cu+8HNO3=3Cu(NO3)2 +2NO↑+4H2O 3NO2+H2O=2HNO3+NO 缓缓通入![]() mL氧气
mL氧气
【解析】
(1)①铵盐和碱反应生成氨气,实验室用固体氯化铵和固体氢氧化钙反应制备氨气,反应的方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
②氨气极易溶于水,所以只能用排空气的方法收集,又因为氨气密度小于空气密度,所以选择向下排空气法收集;
③氨气易溶于水,使装置中的压强小于外界的压强,从而引起倒吸;
(2)①b.氨气催化氧化生成一氧化氮和水,化学方程式:4NH3+5O2![]() 4NO+6H2O,氨气中-3价N升高为+2价,体现还原性;
4NO+6H2O,氨气中-3价N升高为+2价,体现还原性;
②铜与稀硝酸反应生成硝酸铜和一氧化氮和水,化学方程式:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,硝酸中+5价N降为+2价,体现氧化性;
(3)①二氧化氮可以和水之间反应,反应物NO2中N元素化合价降低为+2价,升高为+5价,生成硝酸和一氧化氮,反应为:3NO2+H2O=2HNO3+NO;
②NO2与水和氧气反应生成硝酸,发生反应的方程式为:4NO2+O2+2H2O=4HNO3,所以使试管中NO2完全被水吸收的操作是:向试管中通入![]() 氧气。
氧气。


科目:高中化学 来源: 题型:
【题目】高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:

下列说法正确的是 ( )
A. 自然界中存在大量的单质硅
B. 步骤电弧炉中的化学方程式为SiO2+C![]() Si+CO2↑
Si+CO2↑
C. 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D. SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说法正确的是
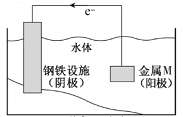
A.阴极的电极反应式为![]()
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制备和收集气体的实验装置合理的是
A.用氯化铵和氢氧化钙制氨气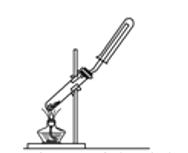
B.用铜片和稀硝酸制NO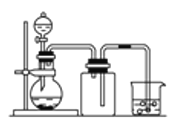
C.用锌粒和稀硫酸制氢气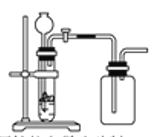
D.用双氧水和二氧化锰制氧气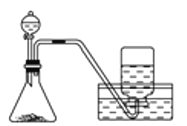
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维拉帕米(又名异搏定)是治疗心绞痛和原发性高血压的药物,合成路线中某一步骤如图所示,下列说法中正确的是
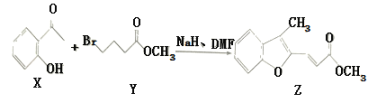
A. Y的分子式为C5H11O2 Br
B. 含苯环和羧基的ⅹ的同分异构体有4种
C. 可以用酸性高锰酸钾溶液鉴别X和Z
D. 1mol Z最多可与6mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验室制取气体的反应中,其原理不属于氧化还原反应的是( )
A.实验室中用稀硫酸与锌粒反应制取 H2
B.实验室中用高锰酸钾加热分解制取 O2
C.实验室中用浓盐酸与二氧化锰加热制取Cl2
D.实验室中用稀盐酸与石灰石反应制取CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氧化还原反应中,氧化剂__电子,发生的反应是__反应;还原剂__电子,发生的反应是__反应。铁与氯气反应的方程式为__,生成物中铁是__价,铁与盐酸的反应化学方程式为___,生成物中铁是___价,这一事实证明,氯气的氧化性比盐酸的氧化性__(填“强”或“弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() gNa和
gNa和![]() gAl同时加入到足量的水中充分反应,将反应后的溶液稀释、定容为
gAl同时加入到足量的水中充分反应,将反应后的溶液稀释、定容为![]() 下列说法正确的是
下列说法正确的是![]()
A.反应中放出的气体在标准状况下的体积为![]()
B.参加反应的水的质量与加入Al的质量相等
C.所得溶液中![]() 和
和![]() 的物质的量之比为2:1
的物质的量之比为2:1
D.所得溶液中阳离子和阴离子的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在人类的生产和生活中有着广泛的应用,某化学兴趣小组利用图一装置探究氨气的有关性质。
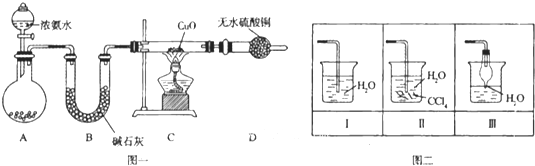
(1)装置A中烧瓶内试剂可选用 (填序号)。B的作用是
a.碱石灰 b.浓硫酸 c.生石灰 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 ,.该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为 mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com