
某化学实验小组需要2mol•L﹣1的NaCl溶液98ml,现用NaCl固体来配制,请回答下列问题:
(1)需称取NaCl11.7g
(2)配制过程中,不需要的仪器(填序号) .
A.药匙 B.酒精灯 C.托盘天平 D.烧杯 E.玻璃棒 F.洗瓶 G.蒸发皿
完成实验还缺少的仪器是 .
(3)在配制过程中,下列操作能引起所配溶液浓度偏低的有 (填序号).
①称量NaCl固体时,砝码与NaCl固体位置放反(1g以下用游码)
②所称取的NaCl固体含有其他杂质 ③转移前,容量瓶中含有少量蒸馏水
④定容时,俯视刻度线 ⑤转移时有少量液体溅出
(4)该实验小组用上述配制的溶液进行如右图所示的电解实验.
①写出该电解反应的化学方程式,并在化学方程式上标出电子转移的方向和数目: ;
②电解时,将Y极(阳极)生成的物质通入盛有NaI溶液的试管中,再加入四氯化碳充分震荡,最后观察到的现象是 .
A.溶液分层,上层无色,下层橙红色
B.溶液分层,上层橙红色,下层无层
C.溶液分层,上层无色,下层紫红色
D.溶液分层,上层紫红色,下层无层
③写出工业用Y极生成的物质来制取漂白粉的化学方程式: 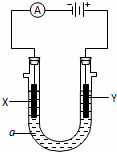
考点: 配制一定物质的量浓度的溶液;电解原理.
分析: (1)根据实验室无98mL的容量瓶,只能选用100mL容量瓶配制出100mL溶液来计算;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(3)根据c=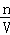 并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(4)①电解饱和食盐水的方程式为2NaCl+2H2O 2NaOH+Cl2↑+H2↑,反应中Cl元素的化合价升高,H元素的化合价降低,每转移2mol电子生成1氯气;依据化学方程式计算.
2NaOH+Cl2↑+H2↑,反应中Cl元素的化合价升高,H元素的化合价降低,每转移2mol电子生成1氯气;依据化学方程式计算.
②阳极上是Cl﹣放电生成Cl2,通入盛有NaI溶液的试管中能将I2置换出,再加入四氯化碳充分震荡则能将碘单质萃取出,根据四氯化碳的密度比水小来分析现象;
③工业上漂白粉是用氯气和石灰乳反应来制取.
解答: 解:(1)实验室无98mL的容量瓶,只能选用100mL容量瓶配制出100mL溶液,故所需的NaCl的质量m=nM=CVM=2mol/L×0.1L×58.5g/mol=11.7g,故答案为:11.7g;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知实验过程中需要托盘天平、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管、洗瓶等仪器,则不需要BG,还缺少100mL容量瓶、胶头滴管,故答案为:BG;100mL容量瓶、胶头滴管;
(3)①称量NaCl固体时,砝码与NaCl固体位置放反(1g以下用游码),会导致药品的质量偏小,则所配溶液的浓度偏低;
②所称取的NaCl固体含有其他杂质,则氯化钠的实际质量偏小,则配制出的溶液的浓度偏低;
③若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响;
④定容时,俯视刻度线,会导致溶液体积偏小,则浓度偏高;
⑤转移时有少量液体溅出,则导致溶质的损失,故所配溶液的浓度偏低.
故选①②⑤;
(4)①电解饱和食盐水的方程式为2NaCl+2H2O 2NaOH+Cl2↑+H2↑,反应中Cl元素的化合价升高2价,H元素的化合价降低2价,反应中转移2个电子,电子转移的方向和数目为:
2NaOH+Cl2↑+H2↑,反应中Cl元素的化合价升高2价,H元素的化合价降低2价,反应中转移2个电子,电子转移的方向和数目为: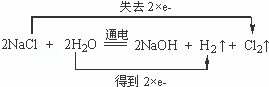 ,
,
故答案为: ;
;
②阳极上是Cl﹣放电生成Cl2,通入盛有NaI溶液的试管中能将I2置换出,再加入四氯化碳充分震荡则能将碘单质萃取出,由于四氯化碳不溶于水且密度比水小,故溶液分层,碘的四氯化碳溶液在下层,呈紫红色,水在上层,呈无色,故选C;
③工业上漂白粉是用氯气和石灰乳反应来制取的,化学方程式为:2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,故答案为:2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;
点评: 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,并考查了电化学的有关知识,综合性较强,但难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
室温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为 ( )。
A.0.01 mol·L-1 B.0.017 mol·L-1
C.0.05 mol·L-1 D.0.50 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案能达到目的是()
A. 除去Fe粉中混有的I2:加热使I2升华
B. 除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶
C. 除去碳酸钠中混有的碳酸氢钠:加入过量的氢氧化钠溶液,蒸发结晶
D. 除去氯气中含有的氯化氢气体:用饱和食盐水洗涤后干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且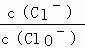 的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是()
的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是()
A. 改变温度,产物中KClO3的最大理论产量为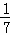 amol
amol
B. 若某温度下,反应后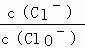 =11,则溶液中
=11,则溶液中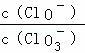 =
=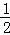
C. 参加反应的氯气的物质的量等于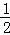 amol
amol
D. 改变温度,反应中转移电子的物质的量ne的范围: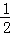 amol≤ne≤amol
amol≤ne≤amol
查看答案和解析>>
科目:高中化学 来源: 题型:
用右图所示装置检验乙烯时不需要除杂的是
| 乙烯的制备 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
| C | CH3CH2OH与浓H2SO4加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | CH3CH2OH与浓H2SO4加热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
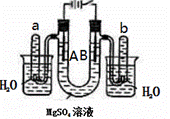
右图是一个用铂丝作电极,电解足量的稀MgSO4溶液的装置.
回答下列问题:
(1)写出A管中发生反应的反应式______________________________________________;
(2)写出B管中发生反应的反应式_________________________________________;
(3)检验a管中气体的方法是___________________________________________________;
(4)检验b管中气体的方法是___________________________________________________;
 (5)电解一段时间后,切断电源,将电解液导入烧杯内观察到的现象是__________________.
(5)电解一段时间后,切断电源,将电解液导入烧杯内观察到的现象是__________________.
(6)电解一段时间后,若加入4.5克水溶液恢复到原来的浓度,则电路中转移电子数目为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化学中的反应类型较多,将下列反应归类(填序号).
①由乙炔制氯乙烯 ②乙烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色
④乙烯使酸性高锰酸钾溶液褪色 ⑤由乙烯制聚乙烯 ⑥甲烷与氯气在光照的条件下反应
⑦乙醇和浓硫酸共热制乙烯 ⑧乙醇和浓硫酸共热得乙醚
其中属于取代反应的是 ;属于氧化反应的是 ;属于加成反应的是 ;属消去反应的是 ;属于聚合反应的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A分子式为CxHyOz,15 g A完全燃烧生成22 g CO2和9 g H2O。
(1)该有机物的最简式为____________________。
(2)若A和Na2CO3混合有气体放出,和醇发生酯化反应,则A的结构简式为____________________________。
(3)若A是易挥发、有水果香味的液体,能发生水解反应,则其结构简式为__________________________________。
(4)若其分子结构中含有6个碳原子,是人体的基本营养物质,则其结构简式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com