
����Ŀ�����������������ڸ����ı����γ�һ�������������ļ������̡�����һ�ְ취�ǽ�������Ʒ�����������ƺ�Ũ�������ƵĻ����Һ�м��ȵ�130�淴Ӧ�����������գ�
(1)�似�������������µĻ�ѧ����ʽ��
��____Fe+____NaNO2+____NaOH��____Na2FeO2+____H2O+____NH3����
��6Na2FeO2 + NaNO2 + 5H2O =3Na2Fe2O4 + NH3�� + 7NaOH��
��Na2FeO2 + Na2Fe2O4 + 2 H2O = Fe3O4 + 4 NaOH��
����ƽ����ʽ�٣����������ת�Ƶķ������Ŀ_____________��
(2)����������������Ӧʱ���ס��ҡ�����λͬѧ������������ǵĿ���������˵����ȷ����_____________��
��ͬѧ�������������в��������Ⱦ����
��ͬѧ��ֻҪ����NaNO2 ����ķ�Ӧ�������dz䵱��������ɫ��
��ͬѧ��ÿһ���������漰���Ļ�ѧ��Ӧ���ɹ�����������ԭ��Ӧԭ��
(3)���������̹����67.2������������£������ת��________mol��
(4)�����1mol Fe3O4����Ӧ������NaOH��������________������������������������________mol��
���𰸡�3 1 5 3 1 1  ��ͬѧ 18 ����
��ͬѧ 18 ���� ![]()
��������
(1)FeԪ�صĻ��ϼ���0����Ϊ+2�ۣ�NԪ�صĻ��ϼ���3�۽���Ϊ-3�ۣ���ϵ��ӡ�ԭ���غ������
(2)������Ⱦ�������٢���NԪ�صĻ��ϼ۽��ͣ�����û��Ԫ�صĻ��ϼ۱仯��
(3)���ð��������ʵ�����NԪ�صĻ��ϼ۱仯����ת�Ƶ��ӣ�
(4)��6Fe+2NaNO2+10NaOH=6Na2FeO2+2H2O+2NH3����6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3��+7NaOH��֪������3mol Na2Fe2O4����3mol NaOH����3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3����֪������3mol Na2FeO2������5mol NaOH��������8mol NaOH����3Na2FeO2+3Na2Fe2O4+6H2O=3Fe3O4+12NaOH�У�����3mol Fe3O4������12mol NaOH��������3mol Fe3O4��������4mol NaOH��
(1)FeԪ�صĻ��ϼ���0����Ϊ+2�ۣ�NԪ�صĻ��ϼ���3�۽���Ϊ-3�ۣ��ɵ��ӡ�ԭ���غ��֪��ӦΪ3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3���������ű�ʾΪ:��
(2)������Ⱦ��������˵�����٢���NԪ�صĻ��ϼ۽��ͣ�����NaNO2����ķ�Ӧ�������dz䵱��������ɫ����˵����ȷ������û��Ԫ�صĻ��ϼ۱仯��������������ԭ��Ӧ��
(3)�а������ɵķ�Ӧ��������NaNO2~ NH3������һ��NH3��ת��6�����ӣ����������̹����67.2������������£������ת��Ϊ![]() =18mol��
=18mol��
(4)��6Fe+2NaNO2+10NaOH=6Na2FeO2+2H2O+2NH3����6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3��+7NaOH��֪������3mol Na2Fe2O4����3mol NaOH����3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3����֪������3mol Na2FeO2������5mol NaOH��������8mol NaOH����3Na2FeO2+3Na2Fe2O4+6H2O=3Fe3O4+12NaOH�У�����3mol Fe3O4������12mol NaOH��������3mol Fe3O4��������4mol NaOH�����������1molFe3O4��Ӧ������NaOH�����������![]() mol NaOH��
mol NaOH��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�IJ����У��е���ͬ���칹�壬�е�û��ͬ���칹�壬����һ��������ͬ���칹��ķ�Ӧ��
A�������ϩ(![]() )������ʵ�����Br2�����ӳɷ�Ӧ
)������ʵ�����Br2�����ӳɷ�Ӧ
B��2�ȶ�����NaOH�Ҵ���Һ���ȷ�����ȥHCl���ӵķ�Ӧ
C���ױ���һ�������·���������Ӧ����һ�����ױ��ķ�Ӧ
D�����ǻ���������NaHCO3��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����÷�ͭм�������������Ʊ�����������ͭ���壩�����̡�
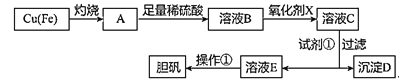
��Һ�б��������� | Fe3+ | Fe2+ | Cu2+ |
��ȫ���������������ʱ����Һ��pH | ��3.7 | ��6.4 | ��4.4 |
��ش�
��1����ҺB�к��е���������__�������ӷ��ţ���
��2��������������������������X����__������ĸ����
A.NaClO B.H2O2 C.KMnO4
д������������Xʱ��������Ӧ�����ӷ���ʽ___��
��3�������Լ�����Ϊ�˵���pH���Լ��ٿ���ѡ��__���ѧʽ����
��֪����������Һ�е�����Ũ��С��1��10-5mol/Lʱ�������ʹ���ȫ����Fe(OH)3���ܶȻ�����Ksp=___��
��4�������ٵIJ��裺___��___�����ˡ�ϴ�ӡ����
��5������D����������Եõ�FeCl3������FeCl3��Һ��������˵������ȷ����__��
A.��FeCl3������Һ��μ����ˮ�У����������ȵõ����ɫҺ�壬��Һ���ܲ��������ЧӦ
B.��FeCl3��Һ�μӵ�����-KI��Һ�У���Һ����ɫ
C.��FeCl3��Һ�������ɲ����գ��õ�FeCl3����
D.��FeCl3��Һ�еμ�KSCN��Һ����Һ�г��ֺ�ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��Ȼ�ѧ����ʽ��������ȷ���ǣ� ��
A.2H2(g)+O2(g)=2H2O(g) ��H=+483.6kJ/mol
B.��֪C(ʯī��s)=C(���ʯ��s) ��H>0������ʯ��ʯī�ȶ�
C.CO(g)��ȼ���ȡ�H=-283kJ/mol����2CO2(g)=2CO(g)+O2(g)��H=+566kJ/mol
D.��֪2C(s)+2O2(g)=2CO2(g) ��H1��2C(s)+O2(g)=2CO(g) ��H2������H1>��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼҵ�е�ⱥ��ʳ��ˮ��ԭ��ʾ��ͼ��ͼ��ʾ(�缫��Ϊʯī�缫)������˵������ȷ����(�� ��)

A. MΪ����������һ��
B. ͨ��ʹ�Ȼ��Ʒ�������
C. ���һ��ʱ���������pH����
D. ���ʱ�����������������pH��2��3�������������ݳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2A+B![]() 3C+4D��Ӧ�У���ʾ�÷�Ӧ���������ǣ� ��
3C+4D��Ӧ�У���ʾ�÷�Ӧ���������ǣ� ��
A.v��A��=0.4mol/��L��s��
B.v��B��=0.3mol/��L��s��
C.v��C��=0.3mol/��L��s��
D.v��D��=2mol/��L��min��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ���ƿ�У���25��ʱ��������ƽ�⣺2NO2(g)![]() N2O4(g) ��H<0������ƿ����100���ˮ�У������м��������в���ı���ǣ� ��
N2O4(g) ��H<0������ƿ����100���ˮ�У������м��������в���ı���ǣ� ��
����ɫ ��ƽ����Է������� ������ ��ѹǿ ���ܶ�
A.�ٺ͢�B.�ۺ͢�
C.�ܺ͢�D.�ں͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ3L���ܱ������з�����ӦCO(g)��2H2(g)![]() CH3OH(g)��CH3OH�����ʵ�����ʱ��仯ͼ����ͼ��
CH3OH(g)��CH3OH�����ʵ�����ʱ��仯ͼ����ͼ��
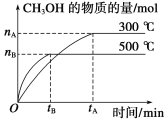
��1���÷�Ӧ��ƽ�ⳣ������ʽK=__��
��2�������¶ȣ�Kֵ��__(����������������С������������)��
��3������ʼʱ����1molCO��2molH2�����ƽ��ʱ��CO��H2��ת����֮��Ϊ__��
��4��500��ʱ���ӷ�Ӧ��ʼ���ﵽ��ѧƽ�⣬��H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ������__(��nB��tB��ʾ)��
��5���жϸÿ��淴Ӧ�ﵽ��ѧƽ��״̬�ı�־��__(����ĸ����ͬ)��
a.CO��Ũ�Ȳ��ٱ仯
b.���������ܶȲ��ٸı�
c.��������ƽ��Ħ���������ٸı�
d.v����(CH3OH)=v����(CO)
��6��300��ʱ�����������ݻ�ѹ����ԭ����![]() ���������������������£���ƽ����ϵ������Ӱ����__��
���������������������£���ƽ����ϵ������Ӱ����__��
a.CH3OH�����ʵ�������
b.����Ӧ���ʼӿ죬�淴Ӧ���ʼ���
c.c(CO)��c(H2)����С
d.����ƽ��ʱ![]() ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���һ�������(C8H16)�����Ʊ���Ȳ(C8H6)���Ȼ�ѧ����ʽ���£�
��C8H16(l)![]() C8H10(l)+3H2(g)����H1��0
C8H10(l)+3H2(g)����H1��0
��C8H10(l)![]() C8H6(l)+2H2(g)�� ��H2��0
C8H6(l)+2H2(g)�� ��H2��0
��1����ͬѹǿ���¶����һ��������ƽ��ת��������ͼ��ʾ��
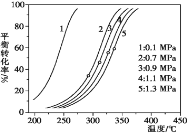
������ͬѹǿ�������¶ȣ�δ�ﵽ��ƽ��ǰ��v��____�������� ������С����������������v����
���о��������������¶�������ѹǿ��C8H16(l)��ת����Ҳ���ߣ����ɿ�����____ ��
��2��t ����������ܱշ�Ӧ���г���1��00 mol C8H16(l)���д����⣬���Һ̬C8H10(l)��C8H6(l)�IJ���x1��x2�������ʵ��������ƣ���ʱ��仯��ϵ����ͼ��ʾ��

����8 hʱ����Ӧ��ϵ����������Ϊ_____mol��������������Ӧ����Һ̬C8H16(l)��ת������_________��
��x1��������x2��ԭ����________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com