
| A. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S | |
| D. | 硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
分析 A.Li燃烧生成Li2O,Na燃烧生成Na2O2,碱金属的性质越活泼,燃烧产物越复杂;
B.卤素单质从上到下颜色加深、状态由气体、液体、固体变化,AgX不溶于水和酸(AgF除外);
C.不能利用氢化物的酸性比较非金属性;
D.位于金属与非金属的交界处的元素,具有金属性和非金属性.
解答 解:A.Li燃烧生成Li2O,Na燃烧生成Na2O2,碱金属的性质越活泼,燃烧产物越复杂,则铷(Rb)的燃烧产物比钠的燃烧产物更复杂,可能有超氧化物,故A正确;
B.卤素单质从上到下颜色加深、状态由气体、液体、固体变化,AgX不溶于水和酸(AgF除外),则砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸,故B正确;
C.不能利用氢化物的酸性比较非金属性,比较角度不合理,应利用氢化物的稳定性比较非金属性,故C错误;
D.位于金属与非金属的交界处的元素,具有金属性和非金属性,则硅、锗都位于金属与非金属的交界处,都可以做半导体材料,故D正确;
故选C.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,选项C为易错点,题目难度不大.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:解答题

| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | $\frac{{N}_{A}}{{V}_{m}}$ | B. | $\frac{M}{m{V}_{m}}$ | C. | $\frac{ρ{N}_{A}}{M}$ | D. | $\frac{ρ{N}_{A}}{m}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H+透过质子交换膜由右向左移动 | |
| B. | 铜电极应与X相连接 | |
| C. | M电极的反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.5 mol气体时,则铁电极增重32 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该方法将电能转化成化学能 | |
| B. | 在此装置中钢管道作正极 | |
| C. | 该方法称为“外加电流的阴极保护法” | |
| D. | 镁块上发生的电极反应为O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
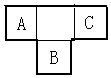 A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.且含B元素物质的大量燃烧是形成酸雨的主要原因之一.
A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.且含B元素物质的大量燃烧是形成酸雨的主要原因之一.  ,用电子式表示元素B的钠盐的形成过程:
,用电子式表示元素B的钠盐的形成过程: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com