
 请完成下列问题
请完成下列问题| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
分析 (1)红磷比白磷稳定,说明红磷能量比白磷低,红磷转化为白磷为吸热反应;
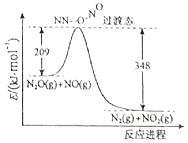
(2)由图可知△H=209kJ/mol-348kJ/mol=-139kJ/mol,结合物质的状态及反应物、生成物书写;
(3)根据三个化学反应方程式可知,反应2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)可由另两个反应变形后加和得到,则由盖斯定律可知,△H3应为另两个反应反应热的加和;
(4)H2(g)+Br2(g)=2HBr(g)△H=-72KJ/mol,结合△H=反应物键能和-生成物键能和来解答.
解答 解:(1)①4P(白磷,s)+5O2(g)=2P2O5(s)△H1;
②P4(红磷,s)+5O2(g)=2P2O5(s)△H2;
①-②得到反应:4P(红磷,s)=P4(白磷,s)△H=△H2-△H2,红磷比白磷稳定,说明红磷的能量低于白磷,该反应是吸热反应,即△H2-△H1>0,即△H2>△H1,
故答案为:<;
(2)该反应中△H=209kJ/mol-348kJ/mol=-139kJ/mol,所以其热化学反应方程式为:N2O(g)+NO(g)=N2(g)+NO2(g)△H=-139kJ•moL-1,
故答案为:N2O(g)+NO(g)=N2(g)+NO2(g)△H=-139kJ•moL-1;
(3)①2H2O(g)═O2(g)+2H2(g)△H1;
②Cl2(g)+H2(g)═2HCl(g)△H2;
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3;
则反应③=2×②+①,
由盖斯定律可知,△H3=△H1+2△H2,
故答案为:A;
(4)H2(g)+Br2(g)=2HBr(g)△H=-72KJ/mol,△H=反应物键能-生成物键能,则有-72=436+200-2a,a=354,
故答案为:354.
点评 该题考查热化学方程式的书写、反应热的计算,是高考中的常见题型,侧重考查学生的分析、计算能力,试题基础性强,难易适中.有利于培养学生学习化学的兴趣,有利于调动学生的学习积极性.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L水中溶解了40 g NaOH后,所得溶液浓度为1 mol/L | |
| B. | 从1 L 2 mol/L的NaCl溶液中取出0.5 L,该溶液的浓度为1 mol/L | |
| C. | 将2.24 L(标准状况)HCl气体溶于水制成100 mL溶液,其物质的量浓度为1 mol/L | |
| D. | 配制1 L 0.2 mol/L的CuSO4溶液,需用32g胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com