
【题目】下列有关说法中不正确的是( )
A. 某温度时的混合溶液中c(H+)=![]() mol·L-1,说明该溶液呈中性
mol·L-1,说明该溶液呈中性
B. 常温下,由水电离出的c(H+)=10-12mol·L-1的溶液的pH可能为2或12
C. 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO42-且浓度均为0.010 mol·L-1溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,CrO42-先产生沉淀
D. 常温下pH=7的CH3COOH和CH3COONa混合溶液中,c(Na+)=c(CH3COO-)
【答案】C
【解析】A.某温度时的混合溶液中c(H+)=![]() molL-1,由于KW=c(H+)c(OH-),说明c(H+)=c(OH-),则溶液一定为中性,A正确;B.25℃时:Kw=c(OH-)×c(H+)=10-14,纯水中c(H+)=c(OH-)=1.0×10-7 mol/L,在25℃时,某溶液中,由水电离出的c(H+)=10-12mol·L-1<10-7mol/L,说明该溶液中的溶质抑制水的电离,溶质能电离出氢离子或氢氧根离子就能抑制水电离,则该溶质可能是酸或碱或强酸的酸式盐,如果为酸溶液,则pH=2,如果为碱溶液,则pH=12,B正确;C.已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,析出沉淀时,AgCl溶液中c(Ag+)=Ksp(AgCl) /c(Cl) =1.56×1010/0.010
molL-1,由于KW=c(H+)c(OH-),说明c(H+)=c(OH-),则溶液一定为中性,A正确;B.25℃时:Kw=c(OH-)×c(H+)=10-14,纯水中c(H+)=c(OH-)=1.0×10-7 mol/L,在25℃时,某溶液中,由水电离出的c(H+)=10-12mol·L-1<10-7mol/L,说明该溶液中的溶质抑制水的电离,溶质能电离出氢离子或氢氧根离子就能抑制水电离,则该溶质可能是酸或碱或强酸的酸式盐,如果为酸溶液,则pH=2,如果为碱溶液,则pH=12,B正确;C.已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,析出沉淀时,AgCl溶液中c(Ag+)=Ksp(AgCl) /c(Cl) =1.56×1010/0.010
mol/L=1.56×10-8mol/L,Ag2CrO4溶液中c(Ag+)=![]() mol/L=3×10-5mol/L>1.56×10-8mol/L,所以Cl-先产生沉淀,C错误;D.常温下pH=7的CH3COOH和CH3COONa混合溶液呈中性,则c(H+)=c(OH-),结合电荷守恒可知:c(Na+)=c(CH3COO-),D正确;答案选C。
mol/L=3×10-5mol/L>1.56×10-8mol/L,所以Cl-先产生沉淀,C错误;D.常温下pH=7的CH3COOH和CH3COONa混合溶液呈中性,则c(H+)=c(OH-),结合电荷守恒可知:c(Na+)=c(CH3COO-),D正确;答案选C。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体。某研究小组用下图所示的实验装置,利用浓氨水、干冰等作原料制备氨基甲酸铵。
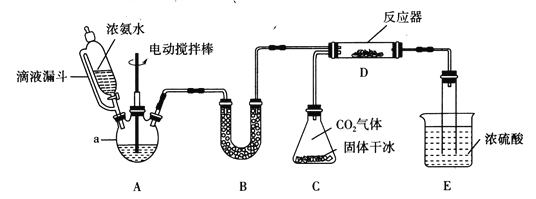
(1)仪器a的名称是____________;与分液漏斗相比,使用滴液漏斗的优点是:______________________________________。
(2)装置B中盛装药品的名称是________________。
(3)写出装置D中发生反应的化学方程式:__________________________________。
(4)装置E的作用之一是控制原料气按反应计量系数充分反应。若反应初期观察到装置内浓硫酸中产生气泡,应该______(填“加快”、“减慢”或“不改变”)产生氨气的流速;装置E的作用还有___________________________________________________。
(5)已知氨基甲酸铵可完全水解为碳酸氢铵。为测定氨基甲酸铵样品的纯度,取样品1.600g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为2.000g。
①写出碳酸氢铵与足量石灰水反应的离子方程式:______________________________。
②样品中氨基甲酸铵的质量分数为_____________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。

请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是_________,滤渣A的主要成分是________。
(2)下列物质中最适合的氧化剂B是______(填字母);反应的离子方程式___________。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲名称分别是:甲______________,乙为常温晾干。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,所加试剂为__(写化学式),能否用酸性的KMnO4溶液?_________填“能”或“否”)理由是:_______。(可用语言或方程式说明)
(5)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba(NO3)2溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2L标准状况下的甲烷和某单烯羟的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了12.6g.该烯羟对氢气的相对密度为21(相对密度 ![]() )
)
①试确定该烯烃;
②求原混合气体中甲烷与烯烃的物质的量之比以及质量之比.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的CH4和NH3相比较,下列结论错误的是
A. 它们的分子个数比为17:16 B. 它们的原子个数比为17:16
C. 它们的氢原子个数比为17:12 D. 它们所含氢元素的质量比为17:12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关食物中营养素的说法正确的是( )
A.维生素C能防治坏血病B.摄入过多的淀粉不会发胖
C.油脂的成分是高级脂肪酸D.蛋白质水解的最终产物是葡萄糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com