
| A. | ①②③ | B. | ②⑤⑥ | C. | ②③⑥ | D. | ④⑤⑥ |
分析 ①标准状况下,1L HCl的物质的量为$\frac{1L}{22.4L/mol}$=$\frac{1}{22.4}$mol,而1L H2O的物质的量为:$\frac{1×1000}{18}$=55.5mol,结合N=nNA分析解答;
②标准状况下,1g H2的物质的量为:$\frac{1g}{2g/mol}$=0.5mol,14g N2的物质的量为:$\frac{14g}{28g/mol}$=0.5mol,根据V=nVm分析解答;
③状况不知无法求体积;
④两种物质的物质的量相同的气体,则它们在标准状况下的体积也相同;
⑤根据PV=nRT分析解答;
⑥根据PV=nRT分析解答.
解答 解:①标准状况下,1L HCl的物质的量为$\frac{1L}{22.4L/mol}$=$\frac{1}{22.4}$mol,而1L H2O的物质的量为:$\frac{1×1000}{18}$=55.5mol,所以物质的量越大,分子数越多,后者大于前者,故错误;
②标准状况下,1g H2的物质的量为:$\frac{1g}{2g/mol}$=0.5mol,14g N2的物质的量为:$\frac{14g}{28g/mol}$=0.5mol,根据V=nVm,物质的量相同气体体积相同,故正确;
③状况不知无法求体积,所以无法求气体的体积,故错误;
④两种物质的物质的量相同的气体,则它们在标准状况下的体积也相同,但物质的状态不知所以无法求体积的大小,故错误;
⑤根据PV=nRT,在同温同体积时,气体物质的物质的量与压强成正比,物质的量越多压强越大,故正确;
⑥根据PV=nRT,可知:PM=ρRT,所以在同温同压下,气体的密度与气体的相对分子质量成正比,故正确;
故选B.
点评 本题考查阿伏伽德罗定律及其推论,注意根据PV=nRT理解阿伏伽德罗定律及其推论、温度及压强对气体摩尔体积的影响,难度中等.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
| A. | σ键就是单键,π键就是双键 | |
| B. | π键是由两个p轨道“肩并肩”重叠形成的 | |
| C. | 乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键 | |
| D. | CO2分子中σ键和π键的数目比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
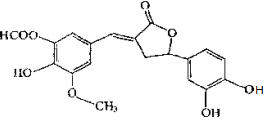
| A. | X分子中含1个手性碳原子 | |
| B. | X能与NaHCO3反应放出二氧化碳 | |
| C. | X能发生缩聚、消去、银镜反应 | |
| D. | 1 mol X最多能与含4 mol Br2的浓溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Pb电极b为阴极 | B. | 阴极的反应式为:N2+6H++6e-=2NH3 | ||
| C. | H+由阳极向阴极迁移 | D. | 陶瓷可以隔离N2和H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸 | B. | Na2CO3 | C. | SO2 | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 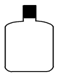 | C. | 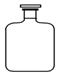 | D. | 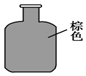 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车排放的尾气和冬季取暖排放的颗粒污染物是形成雾霾的一个因素 | |
| B. | 泡沫灭火器中用的是小苏打和硫酸铝 | |
| C. | 用活性炭为糖浆脱色和用臭氧漂白纸浆,二者所用原理相同 | |
| D. | 从海水中可提取镁,电解熔融氯化镁可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
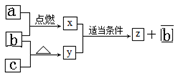 A、B、C、D是原子序数依次增大的第二、三周期主族元素,A、B、C的单质(用a、b、c表示)及其化合物x、y、z有如下转化关系,D与B同主族,下列说法正确的是( )
A、B、C、D是原子序数依次增大的第二、三周期主族元素,A、B、C的单质(用a、b、c表示)及其化合物x、y、z有如下转化关系,D与B同主族,下列说法正确的是( )| A. | x、y、z均是离子化合物 | |
| B. | 简单氢化物的沸点:C>B>D | |
| C. | 最高价氧化物对应的水化物的酸性:A>D | |
| D. | 简单离子半径:D>C>B |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
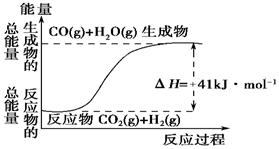
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com