
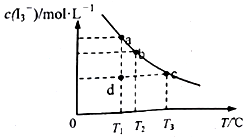
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)═I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)═I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是( )| A. | 温度为T1时,向该平衡体系中加入KI固体,平衡正向移动 | |
| B. | 反应I2(aq)+I-(aq)═I3-(aq)△H<0 | |
| C. | 若T1时,反应进行到状态d时,一定有v正>v逆 | |
| D. | 状态a与状态b相比,状态b时I2的转化率更高 |
分析 A.加入KI固体,c(I-)增大;
B.由图可知,温度越高,c(I3-)越小,则升高温度,平衡逆向移动;
C.T1时,反应进行到状态d时,c(I3-)小于平衡时浓度,则平衡向正反应方向移动;
D.a、b均为平衡点,a点温度低,结合选项B分析.
解答 解:A.加入KI固体,c(I-)增大,则平衡正向移动,故A正确;
B.由图可知,温度越高,c(I3-)越小,则升高温度,平衡逆向移动,可知正反应为放热反应,△H<0,故B正确;
C.T1时,反应进行到状态d时,c(I3-)小于平衡时浓度,则平衡向正反应方向移动,则一定有v正>v逆,故C正确;
D.a、b均为平衡点,a点温度低,该反应为放热反应,降低温度,平衡正向移动,则状态a时I2的转化率更高,故D错误;
故选D.
点评 本题考查化学平衡的影响因素,为高频考点,把握温度、浓度对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意图象与平衡移动原理的结合,题目难度不大.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:填空题
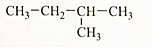
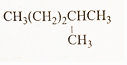 (4)
(4)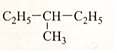 (5)(CH3)2CH-CH2-CH2-CH3.
(5)(CH3)2CH-CH2-CH2-CH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向浓度均为0.1mol•L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 硝酸银溶液中加足量的NaCl溶液,再加KI溶液 | 先得到白色沉淀后变为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | 相同时间内,HA收集到的氢气多 | HA是弱酸 |
| D | 用洁净的铂丝蘸待测液进行焰色反应 | 火焰呈黄色 | 溶液中含Na+,不含K+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
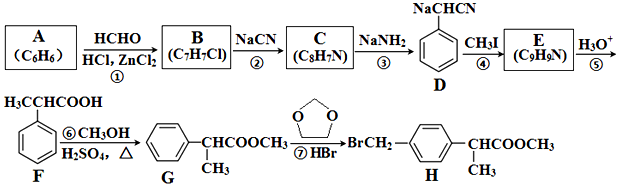
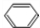 +HCHO+HCl $\stackrel{ZnCl_{2}}{→}$
+HCHO+HCl $\stackrel{ZnCl_{2}}{→}$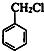 +H2O;反应⑥的化学方程式为
+H2O;反应⑥的化学方程式为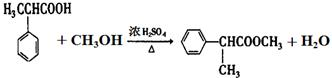 .
.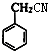 ;E的结构简式为
;E的结构简式为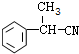 .
. .
.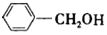 合成
合成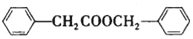 的合成
的合成 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1 molCO、2 mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 衡 时 数据 | CH3OH的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | bkJ | ckJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | a1 | a2 | a3 | |
| A. | 2 c1>c3 | B. | |a|+|b|=90.8 | C. | 2 p2<p3 | D. | a1+a3<1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的电子式: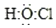 | |
| B. | 中子数为 20 的氯原子:${\;}_{17}^{37}$Cl | |
| C. | 氮原子的结构示意图: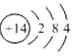 | |
| D. | Na2 S 的水解反应方程式:S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用作净水剂:Fe3++H2O?Fe(OH)3+3H+ | |
| B. | 用于制印刷电路的腐蚀液:2Fe3++Cu═2Fe2++Cu2+ | |
| C. | 与小苏打溶液反应:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑ | |
| D. | 遇KSCN 溶液变红色:Fe3++3SCN-═Fe(SCN)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
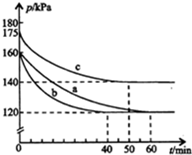 在容积为2L的密闭容器中进行反应:AX3(g)+X2(g)?AX5(g)△H=QkJ/mol,起始时AX3和X2均为1.0mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.下列有关说法不正确的是( )
在容积为2L的密闭容器中进行反应:AX3(g)+X2(g)?AX5(g)△H=QkJ/mol,起始时AX3和X2均为1.0mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.下列有关说法不正确的是( )| A. | Q<0 | |
| B. | 与实验a相比,实验b加入了催化剂 | |
| C. | 实验b条件下,该反应的平衡常数K=2 | |
| D. | 实验c从反应开始至达到平衡时的平均反应速率为v(AX5)=4.0×10-3mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com