
���� ��1�����Ȼ�ѧ����ʽN2��g��+3H2��g��?2NH3��g������H=-92.4kJ•mol-1�ĺ����ǣ���1mol������3mol������ȫ��Ӧ����2mol����ʱ����Ӧ����92.4KJ��
�ڸ��ݻ�ѧƽ��״̬��������𣬵���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯������ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
��2�����ݰ�ˮ�������ɵ�����笠����Ӻ����������ӣ����ƽ��ʱ�����ӵ�Ũ�ȣ������õ���ƽ�ⳣ���ı���ʽ�����NH3•H2O�ĵ���ƽ�ⳣ����
��3������Ksp[Al��OH��3]=1.0��10-33�������������Ũ�ȣ�
��� �⣺��1�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��ʾ1mol������g����3mol������g������2mol������g����Ӧ������Ϊ92.4kJ�����ڸ÷�Ӧ�ǿ��淴Ӧ������1molN2��3molH2��������ȫ��Ӧ�����Էų�����������С��92.4kJ���ʴ�Ϊ��С�ڣ�
��A��NH3���ɵ�������NH3�ֽ��������ȣ��ﵽ��ƽ��״̬����A��ȷ��
B���������ķ�Ӧ����$\frac{2}{3}$v����NH3��=v����H2��������˵�����淴Ӧ������ȣ���һ����ƽ��״̬����B����
C����������������䣬������䣬���Ի��������ܶȲ������ı䣬��״̬��һ����ƽ��״̬����C����
D����λʱ��������a mol N2��ͬʱ����2a mol NH3������˵�����淴Ӧ������ȣ���һ����ƽ��״̬����D����
��ѡA��
��2����ˮ��ҺPH=11����c��H+���T10-11 mol•L-1��c��0H-���T10-3mol•L-1��
NH3•H2O?NH4++OH-
��ʼ��mol•L-1�� 0.1 0 0
��Ӧ��mol•L-1��-��10-3 10-3 10-3
ƽ�⣨mol•L-1�� 0.1 10-3 10-3
NH3•H2O�ĵ���ƽ�ⳣ��Ϊ��$\frac{1{0}^{-3}��1{0}^{-3}}{0.1}$=1.0��10-5��
�����Һ�м����������Ȼ�粒��壬��Һ�������Ũ������ˮ�ĵ���̶ȼ�С����������������Ũ�ȼ�С����ʱ笠����Ӻ�����������Ũ�ȵı�ֵ������
�ʴ�Ϊ��10-5�� ����
��3��0.001mol/LAlCl3��Һ��������Ũ��Ϊ0.001mol/L������Ksp[Al��OH��3]=c��Al3+����[c��OH-��]3�ɵã�c��OH-��=1.0��10-10mol/L�������£�������Ũ��Ϊ��1.0��10-4mol/L����ҺpH=4��
�ʴ�Ϊ��4��
���� ���⿼���˻�ѧƽ��״̬�жϡ����淴Ӧ�ص㡢��ѧƽ�ⳣ���ļ����֪ʶ�������Ѷ��еȣ������漰��֪ʶ��϶࣬ע�����ջ�ѧƽ��״̬���жϷ�������ѧ��Ӧ�Ŀ����ԣ�����ƽ�ⳣ���ļ��㷽����


 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��CaSO4����O2��ȼ��CO��Ӧ���ȿ����ȼ��Ч�ʣ����ܵõ��ߴ�CO2����һ�ָ�Ч����ࡢ���õ�����ȼ�ռ�������Ӧ��Ϊ����Ӧ����Ӧ�ں͢�Ϊ����Ӧ��
��CaSO4����O2��ȼ��CO��Ӧ���ȿ����ȼ��Ч�ʣ����ܵõ��ߴ�CO2����һ�ָ�Ч����ࡢ���õ�����ȼ�ռ�������Ӧ��Ϊ����Ӧ����Ӧ�ں͢�Ϊ����Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��X�ķ�Ӧ����Ϊ0.2 mol•L-1•s-1����Z�ķ�Ӧ����Ϊ0.3 mol•L-1•s-1 | |
| B�� | ���������г��뺤����ѹǿ����Y��ת������� | |
| C�� | �����¶ȣ�����Ӧ���ʼ�С��ƽ�����淴Ӧ�����ƶ� | |
| D�� | ��ʼ���������е�X��Y���ʵ���֮��Ϊ2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ������ | C�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��R��R�����������
��R��R�����������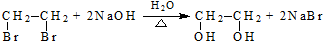 ��
�� ��
��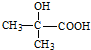 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com