
| A、不能形成酸雨 |
| B、密度比空气的大 |
| C、不能与浓硫酸反应 |
| D、能使品红溶液褪色 |


科目:高中化学 来源: 题型:
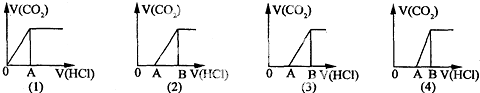
| A、M中只有一种溶质的有(1)和(3) |
| B、M中有两种溶质的有(2)和(4) |
| C、(2)图显示M中含有NaHCO3和Na2CO3两种溶质 |
| D、(4)图显示M中c(NaHCO3)>c(Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在短周期元素中X的金属性最强 |
| B、Y的最高价含氧酸属于弱酸 |
| C、原子半径Z>Y,离子半径Z2->X+ |
| D、Y、Z都可与氢元素形成氢化物,Z的氢化物比Y的氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Ag电极上发生氧化反应 |
| B、盐桥中NO3-向Zn电极移动 |
| C、电子沿Zn→a→b→Ag路径流动 |
| D、片刻后可观察到滤纸a点变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
| A、①④ | B、①③ | C、②③ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、n(Na)+3n(Al)=
| ||
B、aV2=
| ||
| C、35.5aV2=w2-w1 | ||
| D、35.5aV2>(w2-w1) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量却并非是最大值 |
| B、将0.12mol Cl2通入到100mL 1mol/L的FeI2溶液中,离子方程式是:12Cl2+10Fe2++14I-→10Fe3++7I2+24Cl- |
| C、较高的温度下,可以测得0.1mol/L氨水的电离度为55%左右 |
| D、十六烷的裂化产物中不饱和烃的分子数可能会超过50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
 为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.(相对原子质量 C-12 H-1 O-16)
为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.(相对原子质量 C-12 H-1 O-16)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com