
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | a | 945 |
分析 (1)化学反应的焓变=反应物键能总和-生成物键能总和计算;
(2)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=a kJ/mol
②H2O(g)=H2O(l)△H=b kJ/mol
①+②×4得到液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式;
(3)①HCN(aq)?H+(aq)+CN-(aq)△H1,
②H+(aq)+OH-(aq)=H2O(l)△H2=-55.6kJ•mol-1,
③NaOH(aq)+HCN(aq)=NaCN(aq)+H2O(l),△H3=-12.1kJ•mol-1,
盖斯定律计算①+②=③;
(4)根据生成水的质量,利用2H2+O2═2H2O(l)可计算氢气的物质的量,再利用混合气体燃烧放出的热量与氢气燃烧放出的热量来计算CO燃烧放出的热量,最后利用热化学反应方程式来计算CO的物质的量.
解答 解:(1)N2(g)+3H2(g)?2NH3(g)△H=-93kJ•mol-1,化学反应的焓变=反应物键能总和-生成物键能总和,所以得到-93KJ/mol=945KJ/mol+3×436KJ/mol-6×a,解得a=391KJ/mol;
故答案为:391;
(2)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=a kJ/mol
②H2O(g)=H2O(l)△H=b kJ/mol
①+②×4得到液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=(a+4b) kJ/mol;
故答案为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=(a+4b) kJ/mol;
(3)①HCN(aq)?H+(aq)+CN-(aq)△H1,
②H+(aq)+OH-(aq)=H2O(l)△H2=-55.6kJ•mol-1,
③NaOH(aq)+HCN(aq)=NaCN(aq)+H2O(l),△H3=-12.1kJ•mol-1,
盖斯定律计算①+②=③,△H1+△H2=△H3,△H1=+43.5kJ•mol-1,
故答案为:+43.5kJ•mol-1;
(4)水的物质的量为:$\frac{5.4g}{18g/mol}$=0.3mol,
由2H2+O2═2H2O可知,n(H2)=n(H2O)=0.3mol,
由H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.83kJ•mol-1可知,0.3molH2燃烧放出的热量为:285.83kJ/mol×0.3mol=85.749kJ,
则CO燃烧放出的热量为:114.03kJ-85.749kJ=28.281kJ,
设混合气体中CO的物质的量为x,则
2CO(g)+O2(g)=2CO2(g)△H=-565.8kJ•mol-1
2 565.8kJ
x 28.281kJ
解得:x=0.1mol,
即原混合气体中CO的物质的量为0.1mol,
故答案为:0.1mol.
点评 本题考查化学反应能量变化,热化学方程式娥盖斯定律的计算应用,为高考常见题型和高频考点,侧重于学生的分析能力和电化学知识的综合运用,注意把握盖斯定律计算和热化学方程式书写为解答该题的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
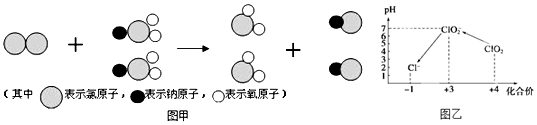
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
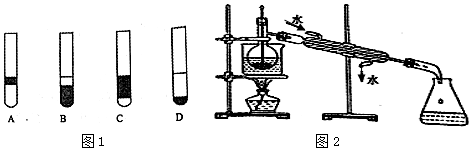
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+) | |
| B. | 如果混合溶液的PH=7,则混合溶液中c(CH3COO-)>c(Na+) | |
| C. | 如果混合溶液的PH<7,则a1b1=a2b2 | |
| D. | 如果a1=a2,且混合溶液的PH<7,则b1>b2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | 只有①④ | C. | 只有②③ | D. | 只有③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L氨水中:c(NH4+)+c(H+)═c(OH-) | |
| B. | 0.1 mol/L的NH4Cl溶液中:c(NH4+)═c(Cl-) | |
| C. | 同为0.1 mol/L的硫酸和氨水等体积混合后:c(NH4+)+c(NH3•H2O)═2c(SO42-) | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-)=c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com