
下列结论均出自《实验化学》中的实验,其中不正确的是
A.硫酸铜溶液中加入过量浓氨水,可得到深蓝色透明溶液
B.NaCl溶液热发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热
C.实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→过滤→氧化→萃取
D.用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在固定相中分配的更多
【知识点】化学实验方案的评价
【答案解析】D 解析:A、硫酸铜溶液中加入浓氨水,先生成氢氧化铜沉淀,氨水过量,可发生络合反应生成溶于水的铜氨络离子,故A正确;B、NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热,防止蒸干,故B正确;C、实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→过滤→氧化(酸化的双氧水)→萃取碘单质,注意氧化剂不能用氯水,防止引入新杂质,故C正确;D、纸上层析法由于样品中各物质分配系数不同,因而扩散速度不同而形成不同位置的色斑,所以色斑的形成和距离可判断分离的效果,滤纸上方颜色呈棕黄色,下方呈深蓝色,据此可知Fe3+在流动相中分配的多一些,随流动相移动的速度快一些;Cu2+在固定相中分配的多一些,随流动相移动的速度慢一些。故D错误;
故答案选D
【思路点拨】本题考查较为综合,涉及蒸发、纸层析法、海带提碘等知识,侧重于考查学生化学实验的评价能力,为高考常见题型,注意把握相关物质的性质,题目难度不大。


科目:高中化学 来源: 题型:
氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等.为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
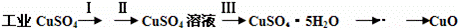
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
(1)步骤Ⅰ的目的是除不溶性杂质.所需操作的名称是 溶解、过滤 .
(2)步骤Ⅱ的目的是除硫酸亚铁.操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1.
①写出用H2O2溶液除去硫酸亚铁的离子方程式 .
②调整pH 的范围应该在 之间.
(3)步骤Ⅲ的目的是得到CuSO4•5H2O晶体.操作是将溶液加热蒸发至有晶膜出现时,停止加热, ,水浴加热烘干.采用水浴加热的原因是 .
(4)该同学用CuSO4溶液进行如下探究实验:
取A、B两支试管,分别加入 2mL 5% H2O2溶液,再向H2O2溶液中分别滴入0.1mol•L﹣1FeCl3和CuSO4 溶液各1mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确 (填正确或错误),请说明原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
肼是重要的化工原料。某探究小组利用下
列反应制取水合肼(N2H4·H2O)。
CO(NH2)2+ 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
实验一: 制备NaClO溶液。(实验装置如右图所示)
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有 (填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2) 锥形瓶中发生反应的化学方程式是 。

(3) 因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液的NaOH的浓
度。请选用所提供的试剂(H2O2溶液、FeCl2溶液、0.1000mol·L-1盐酸、酚酞试液),设计实验方案。
。
实验二: 制取水合肼。(实验装置如右图所示)

控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。
加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。(已知:N2H4·H2O + 2NaClO = N2↑ + 3H2O + 2NaCl)
(4)分液漏斗中的溶液是 (填标号)。
A.CO (NH2) 2溶液 B.NaOH和NaClO混合溶液
选择的理由是 。
实验三: 测定馏分中肼含量。
称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL,用0.1000mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4·H2O + 2I2 = N2↑+ 4HI + H2O)
(5)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是 。
(6)实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4·H2O)的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是
A.用米汤检验含碘盐中的碘酸钾(KIO3)
B.用食醋除去暖水瓶中的薄层水垢
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验过程中的现象及结论均正确且存在因果关系的是

| 实验 | 实验现象 | 结论 |
| A | 广口瓶中光亮的铁钉放置一段时间后生锈 | 铁钉发生析氢腐蚀 |
| B | 左烧杯铝表面冒气泡,右烧杯铜表面冒气泡 | 活动性:Al>Fe>Cu |
| C | 左烧杯气体颜色加深,右烧杯气体颜色变浅 | NO2转化为N2O4吸热 |
| D | 白色固体先变为黄色,后变为黑色 | Ksp:AgCl>AgI>Ag2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
有相同的三块铝片,进行如下实验
实验一:取第一块铝片,直接放入硫酸铜溶液中观察现象
实验二:取第二块铝片,用砂纸擦试表面后,放入硫酸铜溶液中观察现象
实验三:将实验一中铝片从硫酸铜溶液中取出,洗净后放入氢氧化钠溶液中,片刻后取出铝片,洗净后再放入硫酸铜溶液中观察现象
实验四:取第三块铝片,用砂纸擦试表面后,置于浓硝酸中,片刻后取出,洗净,再放入硫酸铜溶液中观察现象综合以上四个实验的主要目的是试图说明
A.铝片表面能形成具有保护作用的氧化膜 B.铝片能和氢氧化钠溶液反应
C.铝片不能和硝酸反应 D.铝片能和硫酸铜溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化合物A的相对分子质量为153,A有如下的性质:
Ⅰ.取A的溶液少许,加入NaHCO3溶液,有气体放出。
Ⅱ.另取A的溶液,向其中加入足量的NaOH溶液,加热反应一段时间后,再加入过量HNO3酸化的AgNO3溶液,有淡黄色沉淀生成。
A有如下的转化:
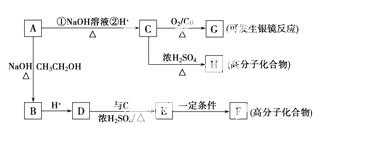
请填空:
(1)A物质的结构简式为_____________________________________________。
(2)C—→G的反应类型为_______________________________________;
A—→B的反应类型为___________________________________________。
(3)写出与C具有相同官能团的同分异构体的结构简式:
_____________________________________________________________;
G与过量的银氨溶液反应,每生成2.16 g Ag,消耗G的物质的量是________ mol。
(4)写出下列反应的化学方程式:
D—→E______________________________________________________;
C—→H__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
混凝土强度大,常常用来建造高楼大厦、桥梁涵洞、高速公路等,在现代社会中发挥着举足轻重的作用,下面是钢筋混凝土的主要成分的是( )
A.水泥、沙子和钢筋 B.水泥、沙子、碎石和钢筋
C.水泥、碎石和钢筋 D.水泥、沙子和碎石
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源。
(1)在汽车尾气系统中安装催化转换器,可有效减少尾气中的CO、NOx 和碳氢化合物等废气。
已知:N2(g)+O2(g)=2NO(g) △H1=+180kJ/mol
CO(g) +1/2O2(g)= CO2(g) △H2=-283kJ/mol
2NO(g)+ 2CO(g) = 2CO2(g) + N2(g) △H3
则△H3 = kJ·mol-1。
(2)气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g) △H >0
2NO(g) △H >0
①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,原因是 。
②1mol空气中含有0.8molN2和0.2molO2,1300℃时在含1mol空气的密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K≈ 。
(3)尾气中的CO主要来自于汽油不完全燃烧。
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g) △H=+221kJ·mol-1,简述该设想能否实现的依据: 。
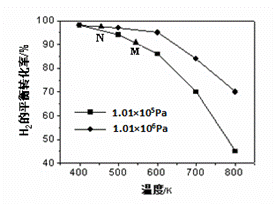 ②测量汽车尾气的浓度常用电化学气敏传感器,其中CO传感器可用下图简单表示,则阳极发生的电极反应为 。
②测量汽车尾气的浓度常用电化学气敏传感器,其中CO传感器可用下图简单表示,则阳极发生的电极反应为 。
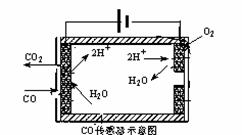
(4)汽车尾气中的CO可转化为甲烷,方程式为CO(g)+3H2(g) CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
①该反应的△H 0(填“<”、“=”或“>”)。
②实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com