
 ʵ���������Ҵ���Ũ�����170����������ȡ��ϩ�ģ�
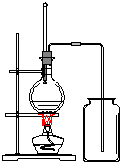
ʵ���������Ҵ���Ũ�����170����������ȡ��ϩ�ģ����� ��1������Ũ�������170�淢����ȥ��Ӧ������ϩ���壻
��2�����ݷ�Ӧ����ʽ���Ҵ�����ϩ֮�����Ĺ�ϵ�����㼴�ɣ�
��3����Ӧ���Һ�¶�Ѹ�����ߵ�170�����Ʊ���ϩ����ϩ�ܶȺͿ���������ݴ˻ش�
��� �⣺��1���Ҵ���Ũ�������170�淢����ȥ��Ӧ������ϩ���壬��Ӧ�Ļ�ѧ����ʽΪCH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O���ʴ�Ϊ��CH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O��
��2���Ҵ���Ũ�������170�淢����ȥ��Ӧ������ϩ���壬��Ӧ�Ļ�ѧ����ʽΪCH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O��Ҫ��ȡ1.4g ��0.05mol��ϩ����Ҫ�Ҵ���������0.05mol��46g/mol=2.3g������������Ҫ�Ҵ�����=0.79g/mL������Ϊ$\frac{2.3g}{0.79g/mL}$=2.9mL���Ҵ���140�淢������Ӧ���Ҵ��ӷ����Ҵ���Ũ����������ԭ�����Ҵ�ʵ�ʵ�ʹ����Ҫ����2.9���ʴ�Ϊ��2.9���Ҵ���140�淢������Ӧ���Ҵ��ӷ����Ҵ���Ũ���������ȣ�
��3����ȡ���ռ���ϩװ���е���������Ӧ���Һ�¶�Ѹ�����ߵ�170�棬�����¶ȼƵ�ˮ������뷴ӦҺ���£���ϩ�ܶȺͿ��������Ӧ������ˮ���ռ���
�ʴ�Ϊ���¶ȼƵ�ˮ����û�в��뷴ӦҺ����ϩӦ������ˮ���ռ���
���� ���⿼�����Ҵ��Ļ�ѧ���ʵ�Ӧ�ã���Ӧ�����и���Ӧ�ķ����ж��ǽ���ؼ���ע��֪ʶ�Ļ��ۣ���Ŀ�ϼ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol H+���еĵ����� | |
| B�� | ��״���£�22.4L�ƾ������ķ����� | |
| C�� | 1.6 g CH4 ��������� | |
| D�� | 1L 1mol/L����������Һ������Na+ �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
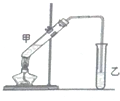 ��˵�����¾��ϴ��ر��㡱����ԭ���Ǿ��ڴ������������������ζ��������������ʵ����������Ҳ��������ͼ��ʾ��װ����ģ��ù��̣���ش��������⣺
��˵�����¾��ϴ��ر��㡱����ԭ���Ǿ��ڴ������������������ζ��������������ʵ����������Ҳ��������ͼ��ʾ��װ����ģ��ù��̣���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
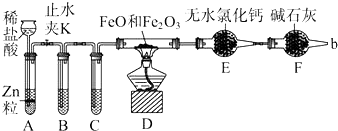
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
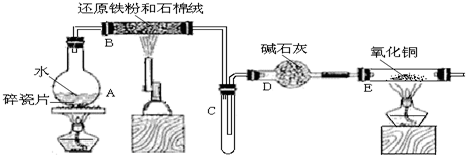
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
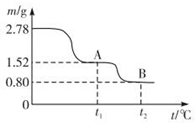
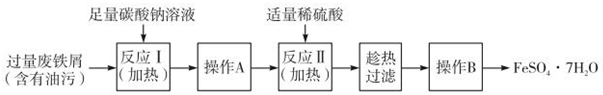
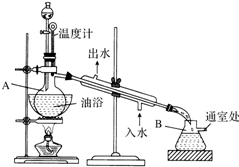 ������������ɫ����ˮ����ζ��Һ�壬�е�77.1�棬ij����ȡʵ���õ�������14.3mL��95%�Ҵ�23mL�����õ�ŨH2SO4������Na2CO3��Һ�Լ��������Ҵ���ϳ�����������Ȼ�����Һ����Ҫ����װ����ͼ��ʾ��ʵ�鲽���ǣ�
������������ɫ����ˮ����ζ��Һ�壬�е�77.1�棬ij����ȡʵ���õ�������14.3mL��95%�Ҵ�23mL�����õ�ŨH2SO4������Na2CO3��Һ�Լ��������Ҵ���ϳ�����������Ȼ�����Һ����Ҫ����װ����ͼ��ʾ��ʵ�鲽���ǣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
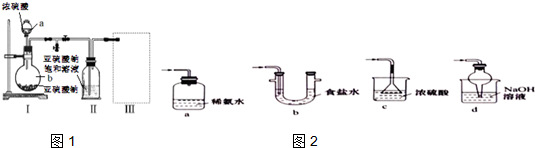
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
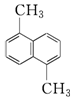 ����A�ķ���ʽΪC12H12���ṹ��ʽΪ��ͼ����֪�����ϵĶ��������9��ͬ���칹�壬�ɴ��Ʋ�A�ı����ϵ����������칹����Ŀ�У�������
����A�ķ���ʽΪC12H12���ṹ��ʽΪ��ͼ����֪�����ϵĶ��������9��ͬ���칹�壬�ɴ��Ʋ�A�ı����ϵ����������칹����Ŀ�У�������| A�� | 9�� | B�� | 10�� | C�� | 11�� | D�� | 12�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com