
【题目】化学与生产、生活密切相关,下列说法正确的是( )
A.明矾作为净水剂,可以除去废水中的铜离子
B.焰火的五彩缤纷是某些金属元素化学性质的展现
C.用活性炭为蔗糖脱色和用臭氧漂白纸浆的原理相同
D.工业上以氯气和石灰乳为原料制备漂白粉
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】分析下表中各项的排布规律,按此规律排布第23项应为
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C2H6 | C2H4 | C2H4O2 | C3H8 | C3H6 | C3H6O2 | C4H10 | C4H8 | C4H8O2 | C5H12 |
A.C8H18 B.C9H118O2 C.C9H18 D.C8H16O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
A.乙炔 B.丙炔 C.丁炔 D.丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少 8%,氮氧化物(NOx)排放量减少 10%。目前,消除大气污染有多种方法。
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g)△H =-574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)△H =-1160 kJ/mol
③H2O(g) = H2O(l) △H =-44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式:__________。
(2)利用 Fe2+、Fe3+的催化作用,常温下可将 SO2 转化为 SO42-,从而实现对 SO2 的治理。已知含 SO2 的废气通入含 Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为 4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O,则另一反应的 离子方程式为__________。
(3)用活性炭还原法处理氮氧化物。有关反应为 C(s) + 2NO(g) ![]() N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度(mol/L) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10~20 min 以υ(N2)表示的反应速率为__________。
②该反应的平衡常数表达式 K=________。根据表中数据,计算 T1 ℃时该反应的平衡常数为__________(保留两位小数)。
③一定温度下,随着 NO 的起始浓度增大,则 NO 的平衡转化率__________ (
④下列各项能作为判断该反应达到平衡的是__________ (填序号)。
A.混合气体的密度保持不变
B.υ正(NO) = 2υ逆(CO2)
C.容器内压强保持不变
D.容器内 N2 的体积分数保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为__________,物质的量之比为__________,原子总数之比为__________,质量之比为__________,密度之比为__________。
(2)在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,所含分子数最多的是________,含原子数最多的是________,质量最大的是________,体积最小的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 表示阿伏加德罗常数的值,下列叙述正确的是
A.在反应 KClO3 + 6HCl = KCl + 3Cl2↑+ 3H2O 中,Cl2 既是氧化产物又是还原产物,当得到标准状况下的 67.2 L Cl2 时,反应中转移的电子数为 5NA
B.标准状况下,22.4 L 甲苯中含有的 C—H 键数目为 8NA
C.50 g 46%的乙醇水溶液中,含氢原子总数目为 3NA
D.t℃时,MgCO3 的 Ksp = 4×10-6,则该温度下饱和 MgCO3 溶液中含有的 Mg2+数目为 2×10-3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在周期表中,第3、4、5、6周期元素的数目分别是( )
A. 8、18、32、32 B. 8、18、18、32
C. 8、18、18、18 D. 8、8、18、18
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol MnO2粉末加入到50mL过氧化氢溶液(H2O2,ρ=1.1g/mL)中,在标准状况下放出气体的体积和时间的关系如图所示.
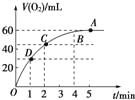
(1)实验时放出气体的总体积是 .
(2)放出一半气体所需的时间为 .
(3)反应放出![]() 体积气体所需的时间约为 .
体积气体所需的时间约为 .
(4)A,B,C,D各点反应速率的快慢顺序为
(5)解释反应速率变化的原因:
(6)计算H2O2初始状态的浓度 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com