
| A. | B. | C. | D. |
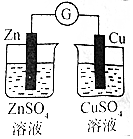 |  |  |  |
| 验证化学能转化为电能 | 验证氧化性:Cl2>Br2>I2 | 验证温度对平衡移动的影响 | 制取MgCl2固体 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.该装置没有形成闭合回路,无法构成原电池;
B.氯气能够氧化碘化钾,干扰了检验结果;
C.根据混合气体的颜色变化可验证温度对化学平衡的影响;
D.HCl易挥发,最终得到的是氧化镁固体.
解答 解:A.装置中缺少盐桥,没有形成闭合回路,无法验证化学能转化为电能,故A错误;
B.剩余的Cl2能够氧化KI,干扰了溴单质与碘化钾的反应,无法达到实验目的,故B错误;
C.升高温度平衡向生成NO2的方向移动,气体颜色加深,可验证温度对平衡移动的影响,故B正确;
D.镁离子水解生成氢氧化镁和HCl,氯化氢易挥发,加热灼烧后最终得到MgO,应该在HCl气流中加热,故D错误;
故选C.
点评 本题考查化学实验方案的评价,题目难度中等,涉及化学平衡及其影响、氧化还原反应、盐的水解原理应用等知识,明确化学平衡及其影响为解答关键,试题有利于提高学生的分析能力及化学实验能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届内蒙古高三上月考二化学试卷(解析版) 题型:选择题
高铁酸钠(Na2FeO4)是一种新型净水剂,制取Na2FeO4的离子方程式为:Fe3+ + OH—+ Cl2 → FeO42—+ Cl— + H2O,该反应配平的离子方程式中H2O的系数是
A.4 B.6 C.8 D.10
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
下列叙述错误的是( )
A.10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49%
B.配制0.1mol/L的Na2CO3溶液480ml,需用500ml容量瓶
C.在标况下,将22.4L氨气溶于1L水中,得到1mol/L的氨水
D.向两等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:
如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +3Br2→
+3Br2→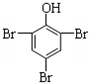 ↓+3HBr;反应类型取代反应.
↓+3HBr;反应类型取代反应. ;反应类型取代反应.
;反应类型取代反应. ;反应类型加聚反应.
;反应类型加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②④⑤ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:X>W>Y>Z | B. | 原子半径:W>X>Z>Y | ||
| C. | 氧化性:X+>W3+ | D. | 氢化物稳定性:HZ>H2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  提取海带中的碘 | B. |  检验火柴燃烧产生的SO2 | ||
| C. |  测定一定时间内生成H2的反应速率 | D. |  证明非金属性Cl>C>Si |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com